Edematózní ledviny
Úvod
Bilaterální zvětšené ledviny jsou charakteristickým nálezem u nejrůznějších onemocnění, např. u akutní či subakutní glomerulonefritidy, pyelonefritidy, amyloidózy, při nefrotickém syndromu, lymfomu, metastatickém postižení nebo při polycystické chorobě ledvin.1
Široká diferenciální diagnostika musí být korelována s klinickými příznaky a laboratorními výsledky konkrétního pacienta, aby byla správně stanovena definitivní diagnóza.
Kazuistika
Jednalo se o 76letou pacientku s anamnézou chronické lymfocytární leukemie (KS Rai I, Binet A, CD38 negativní, diagnostikována 2/2017) po terapii rituximabem, cyklofosfamidem a dexametazonem v roce 2019 s dosažením kompletní remise. Od 21. září do 31. prosince 2021 byla léčena prednisonem pro paraneoplastické projevy s dobrým efektem.
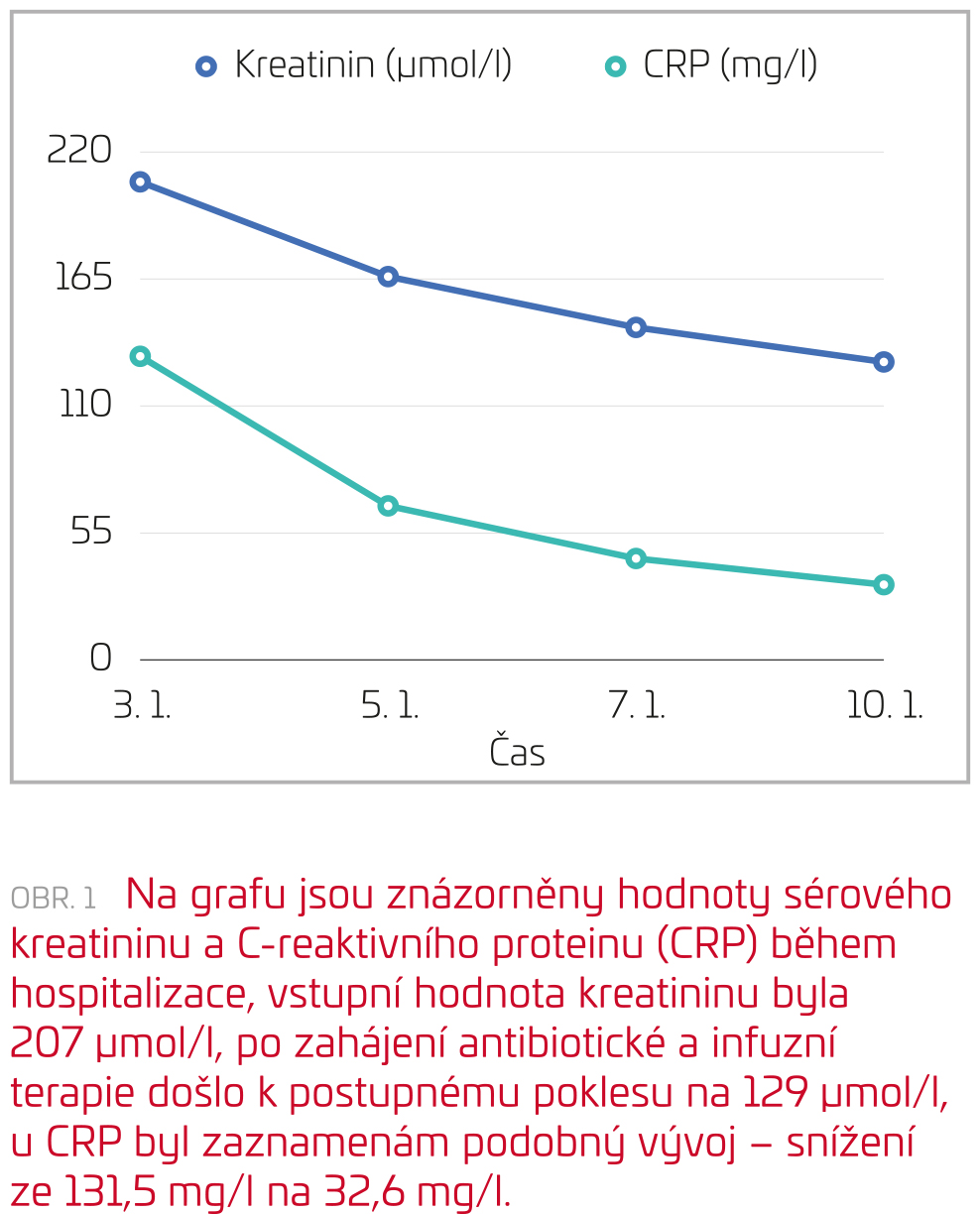
Od 2. ledna do 10. února 2022 byla pacientka hospitalizována na Hematologické klinice FNKV. Pacientka byla nejdříve ošetřena ambulantní cestou pro febrilie po dlouhodobé kortikoterapii. Byly odebrány kultivace a pacientka byla odeslána domů s empirickou antibiotickou terapií, pro přetrvávající febrilie a při hlášené pozitivitě hemokultur však byla hospitalizována k parenterální antibiotické terapii a infuzní hydratační terapii. Během hospitalizace byla doplněna abdominální ultrasonografie, kde kromě lymfadenopatie v horní části retroperitonea a progrese splenomegalie bylo popsáno relativní zvětšení obou ledvin (nález může odpovídat odeznívající bilaterální pyelonefritidě) (obr. 1).
Závěrečné diagnostické shrnutí při dimisi z hematologické kliniky znělo urosepse při bilaterální pyelonefritidě s akutním renálním poškozením a s postupnou úpravou renálních funkcí po terapii, etiologicky se jednalo o infekci Escherichia coli dobře citlivou na antibiotickou terapii. Před hospitalizací měla pacientka normální renální funkce, proto byla doporučena nefrologická dispenzarizace.
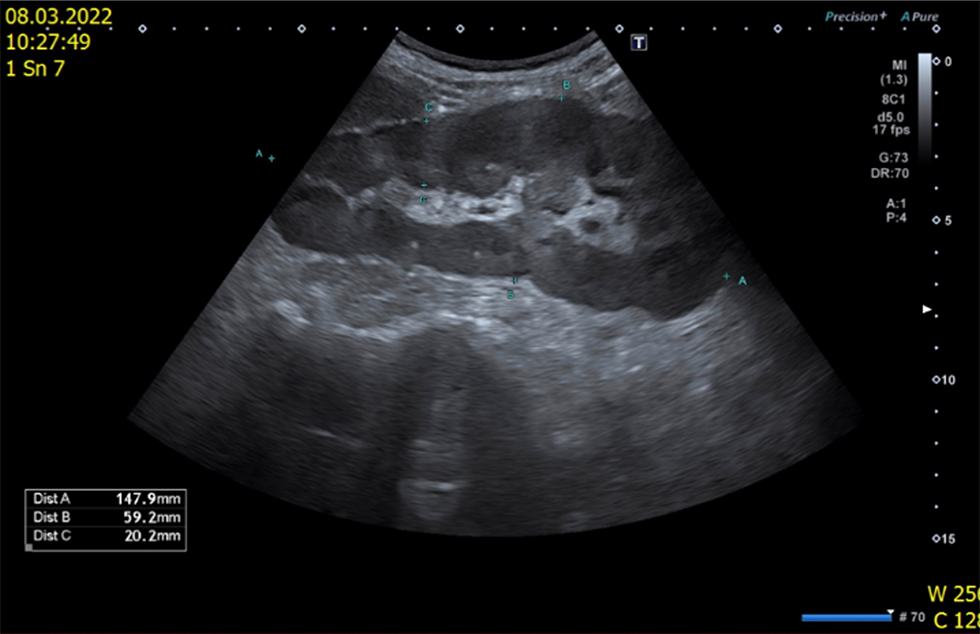
Od 18. do 30. března 2022 byla naše pacientka hospitalizována na Interní klinice FNKV na doporučení ambulantního nefrologa pro kultivačně zjištěnou uroinfekci, avšak tentokrát byla prokázána etiologicky Pseudomonas aeruginosa citlivá pouze na parenterální antibiotickou terapii. Pacientka byla klinicky zcela bez příznaků (bez horečky či dysurických obtíží). Ve farmakologické anamnéze figurovalo železo, inhibitor protonové pumpy a alopurinol. Byla doplněna ultrasonografie břicha (obr. 2) s příznaky zánětlivého postižení obou ledvin jako nepřímými známkami akutní pyelonefritidy. Pacientka byla léčena piperacilinem s tazobaktamem a dále pro záchyt arteriální hypertenze byl do terapie nově přidán blokátor kalciových kanálů (obr. 3).
OBR. 2 Zobrazení ledviny naší pacientky na USG břicha – zvětšené ledviny, bilaterálně podélně 14,0 cm, parenchym na obou ledvinách difuzně rozšířen na 14–19 mm, nepravidelně hypoechogenní.
Etiologie opětovného akutního renálního poškození nebyla již dobře vysvětlitelná infekcí a dehydratací. Shodli jsme se na tom, že v rámci diferenciální diagnostiky pacientce provedeme renální biopsii.
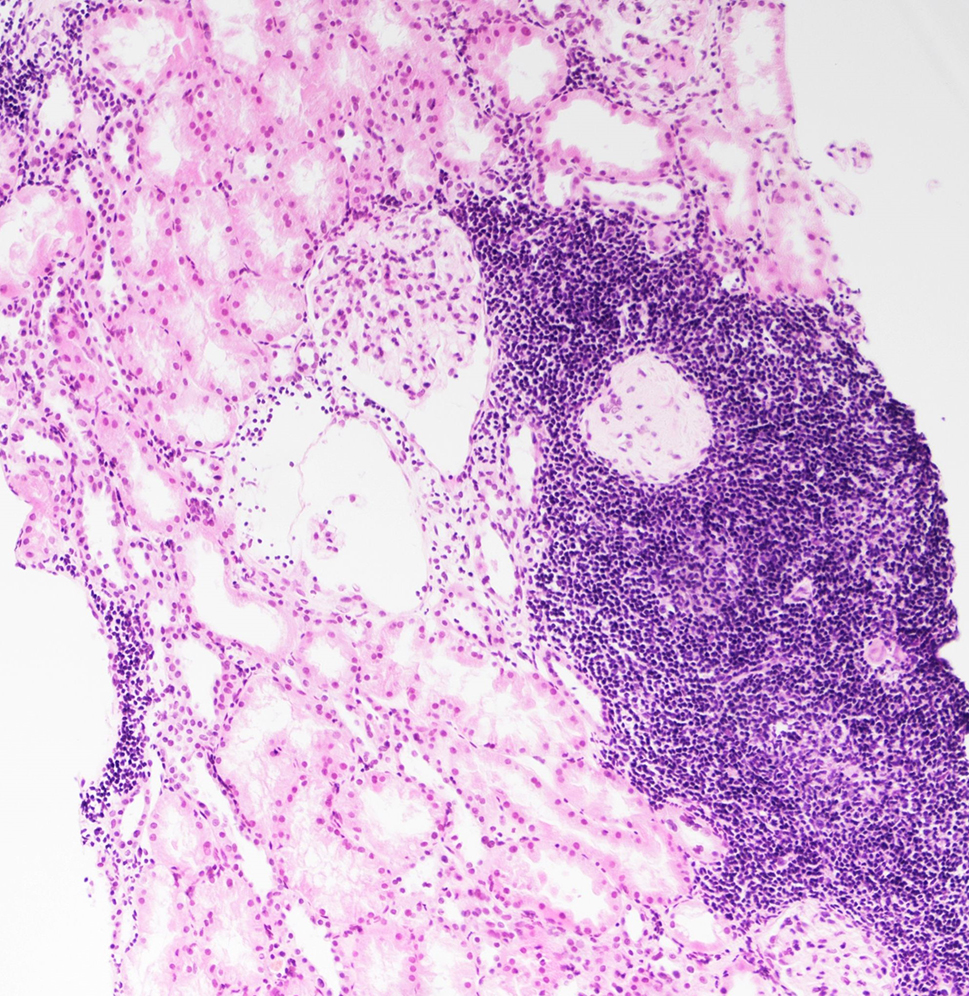
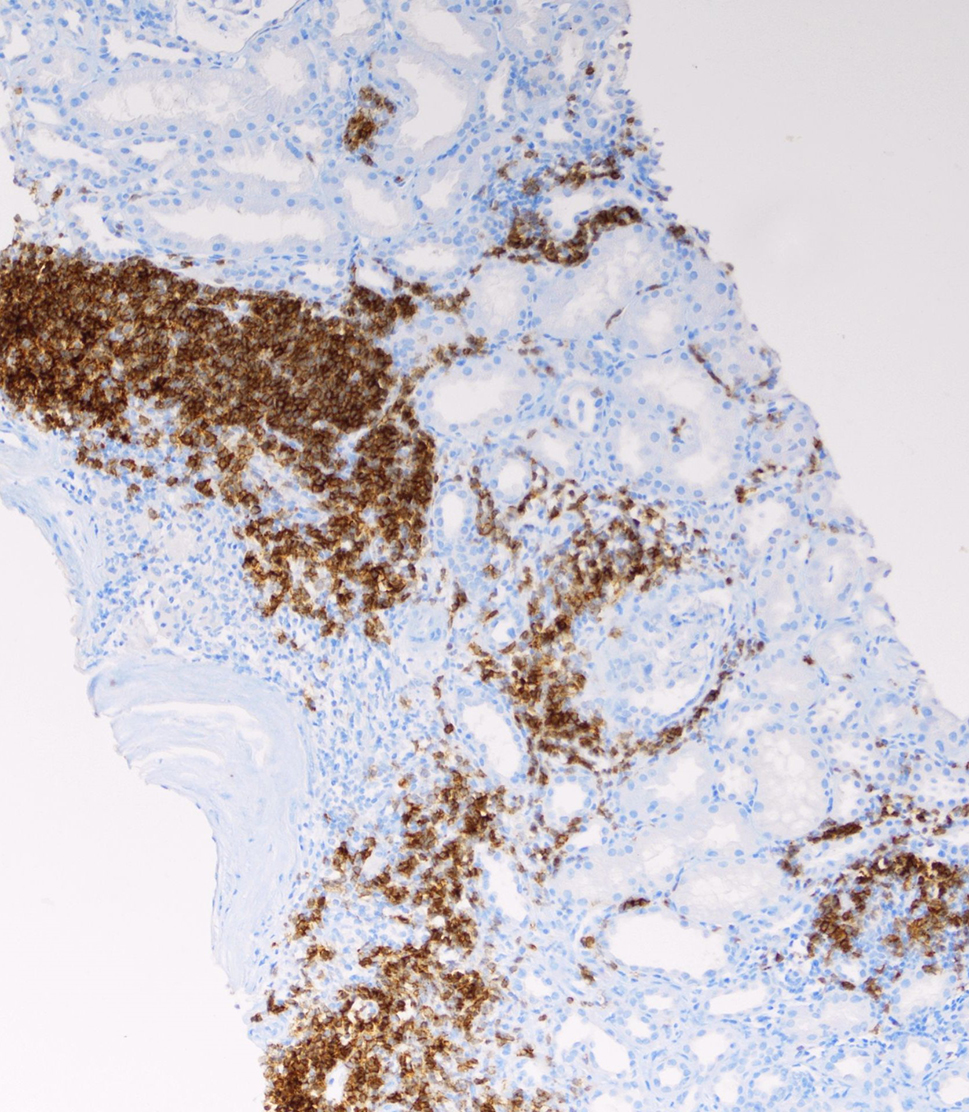
Biopsie ledviny byla rozdělena pro světelnou mikroskopii, imunofluorescenci (IF) a vyšetření elektronovým mikroskopem (ELMI). Ve vzorku pro IF bylo šest glomerulů. Detekce imunoglobulinů (IgG, IgA, IgM), frakcí komplementu (C3, C1q) a lehkých řetězců (kappa, lambda) byly negativní. Ve vzorku pro světelnou mikroskopii byl úsek kůry s juxtamedulární oblastí, celkem s osmi až deseti glomeruly. Morfologie glomerulů byla přiměřená, bez proliferace. V intersticiu kůry i v přilehlém pouzdře ledviny byly ložiskové monotónní infiltráty z malých lymfocytů (obr. 4), v juxtamedulární oblasti byl infiltrát místy prakticky difuzní. Imunofenotyp buněk infiltrátu jsme verifikovali imunohistochemickou detekcí CD20, CD5 a CD23 s pozitivním výsledkem (obr. 5).
OBR. 4 Subkapsulární oblast ledviny s monotónním infiltrátem z malých lymfocytů v okolí zaniklého glomerulu. Zachovalý glomerulus bez proliferace (barvení HE, zvětšení objektiv 10×).
OBR. 5 Imunohistochemická detekce CD20 pozitivních B lymfocytů (aberantní koexprese CD5 a CD23 byla podobného rozsahu, zvětšení objektiv 10×).
Naše konečná diagnóza byla uzavřena jako akutní renální poškození při biopticky verifikované infiltraci ledvin chronickou lymfocytární leukemií s doporučením hematologické revize postupu k další specifické terapii. V ambulantním sledování na naší hematologii bylo rozhodnuto, že po splnění dalších kritérií bude u pacientky indikována specifická terapie inhibitory Brutonovy tyrozinkinázy.
Komentář
Literatura
- Palmer PES (ed.). Manual of diagnostic ultrasound.
- Špaček M, Pospíšilová Š, Doubek M, et al. Doporučení pro diagnostiku a léčbu chronické lymfocytární leukemie (CLL) – 2018. Transfuze Hematol Dnes 2018;24:0–00.
- Wanchoo R, Bernabe Ramirez C, Barrientos J, Jhaveri K. Renal involvement in chronic lymphocytic leukemia. Clin Kidney J 2018;11:670–680.
- Strat P, Nasr SH, Leung N, et al. Renal complications in chronic lymphocytic leukemia and monoclonal B‑cell lymphocytosis: the Mayo Clinic experience. Haematologica 2015;100:1180–1188.
- Kategorie: Kazuistiky
- Klíčová slova: akutní poškození ledvin; biopsie; edematózní ledviny; chronická lymfocytární leukemie; infiltrace ledvin lymfocyty
Chronická lymfocytární leukemie (CLL) je klonální onemocnění CD20 pozitivních B lymfocytů s aberantní koexpresí CD5 a CD23; v klinice s extrémně variabilním průběhem a prognózou.2
Renální postižení u CLL může být klinicky němé nebo se může manifestovat jako akutní renální poškození (AKI) s paraneoplastickým glomerulárním onemocněním (často nefrotickým syndromem), extrarenální obstrukcí nebo jako tumor lysis syndrom. V éře cílených terapií může renální poškození nastat i jako komplikace samotné léčby.3
Pokud pacienti s CLL vyvinou glomerulární onemocnění, v morfologii jde nejčastěji o glomerulonefritidu (GN) s membranoproliferativními rysy, kde definitivní diagnóza zahrnuje kryoglobulinemii, proliferativní GN s monoklonálními depozity, fibrilární i imunotaktoidní GN. V případě nefrotického syndromu (NS) jde především o amyloidózu, membranózní GN a minimal change NS. Pacienti s CLL mají také zvýšené riziko vzniku infekce a autoimunitních onemocnění, proto jsou v průběhu CLL také popisovány GN asociované s infekcemi. V neposlední řadě, protože CLL je většinou onemocněním vyššího věku, patologie nesouvisející s CLL, jako jsou hypertenzní angiopatie, diabetes mellitus, nefropatie, změny v souvislosti s obezitou atd., bude v biopsiích přítomna a může komplikovat morfologickou část diagnózy.
Protože postižení ledvin nepředstavuje dominantní manifestaci, jsou biopsie ledvin u pacientů s CLL prováděny pouze raritně, většina publikovaných dat se odvolává na kazuistiky nebo studie z jednoho centra. Podle obsáhlé studie Mayo Clinic využívající vlastní databázi v kombinaci s publikovanými kazuistikami se mezi nejčastějšími morfologickými postiženími u pacientů s CLL objevuje GN s membranoproliferativními rysy, na druhém místě infiltrace CLL a na třetím místě ve výskytu je minimal change NS.4 Naše kazuistika spadá do druhé nejčastější skupiny.
Patogeneze vzniku AKI u infiltrace ledvin CLL není objasněna, avšak jednou z velmi pravděpodobných příčin je komprese tubulů/mikrovaskulatury, která vede k intrarenální obstrukci a ischemii, v kombinaci se zánětlivou a cytokinovou odpovědí asociovanou s infiltrací. Nejčastější nález na zobrazovacích metodách představuje nefromegalie.3
U naší pacientky byla na počátku velmi pravděpodobně koincidence prodělané urosepse s AKI spolu s infiltrací CLL (při první atace bez bioptické verifikace). Proto další hospitalizace s pozitivní močovou kultivací sváděla k diagnóze rekurence uroinfekce, avšak laboratorní a klinické nálezy při této hospitalizaci nebyly zcela přesvědčivé pro uroinfekci, což vedlo k indikaci biopsie, která odhalila infiltraci CLL. Kazuistika ilustruje důležitost modifikace správnosti vstupního diagnostického závěru během hospitalizace, s průběžnou aktualizací diferenciálně diagnostického postupu s následným stanovením správné diagnózy.