Sepse a její nová definice
Úvod
Infekční příčiny jsou u populace pacientů starších 65 let častějším důvodem hospitalizace než srdeční selhání a infarkt myokardu dohromady.1 U většiny pacientů s infekcí je imunitní, metabolická a hormonální odpověď přiměřená a antimikrobiální léčba je obvykle dostačující k vyléčení. V některých případech však interakce mezi patogenem a hostitelem způsobí nepřiměřenou a deregulovanou odpověď. Důsledkem je rozvoj závažné dysfunkce některých ze životně důležitých orgánů a orgánových systémů. Jinými slovy, prostá infekce se mění v sepsi, která je, na rozdíl od nekomplikované infekce, nositelem mnohem závažnějšího průběhu a celkové prognózy. Sepse je jednoznačně hlavní příčinou úmrtí na infekční choroby. Každoročně na světě postihne 30 milionů pacientů, z nichž 25–30 % zemře.2 Této skutečnosti odpovídají i nedávná data českého multicentrického projektu EPOSS (data‑based Evaluation and Prediction of Outcome in Severe Sepsis), jenž poukazuje na 40% hospitalizační mortalitu pacientů s diagnózou těžké sepse.3 Pacient přijatý s diagnózou sepse má šesti‑ až desetinásobně vyšší riziko úmrtí než pacient s akutním infarktem myokardu a čtyř‑ až pětinásobně vyšší riziko, než pokud by byl přijatý s cévní mozkovou příhodou. Existuje jen málo chorobných procesů s tak vysokou mortalitou. Kvalifikované odhady a epidemiologická data dnes jasně hovoří o sepsi jako o jedné z nejčastějších příčin úmrtí vůbec. Ve vyspělých zemích se počet hospitalizovaných pacientů se sepsí za posledních osm let zdvojnásobil a je vyšší než počet hospitalizací v důsledku infarktu myokardu. Sepse je ve 30–50 % příčinou všech úmrtí v nemocnicích.4 Infekce komplikované rozvojem sepse také velmi negativně ovlivňují výsledky všech páteřních medicínských oborů. U pacientů s chronickým selháním funkce ledvin jsou infekce, respektive sepse, druhou nejčastější příčinou smrti (po kardiovaskulárních příhodách). Zvyšuje se povědomí i o dlouhodobých důsledcích sepse. Pacienti, kteří sepsi přežijí, trpí dlouhodobými tělesnými, mentálními a kognitivními poruchami s významnými zdravotními, sociálními a ekonomickými důsledky a mají zvýšené riziko úmrtí ještě řadu let po epizodě sepse. Finanční náklady, které každé zdravotnictví vynakládá na léčbu sepse během hospitalizace, jsou enormní, dosahují 5,2 % celkových výdajů na zdravotnictví ve vyspělých zemích. V roce 2006 bylo v Evropě vynaloženo na hospitalizace způsobené sepsí odhadem 7,6 miliardy eur. Navzdory těmto alarmujícím číslům zůstává vnímání sepse laickou i odbornou veřejností stále významně ve stínu kardiovaskulárních či onkologických onemocnění.
Nová definice sepse
Urgentní příjmy nemocnic, stejně jako standardní oddělení, jsou častým místem úvodního vyhodnocení septických pacientů. Zřejmou výzvou je proto rozpoznání pacientů s vysokým rizikem progrese stavu nebo úmrtí, především u nemocných, kteří nejsou v úvodu zjevně kriticky nemocní. Podstatná část pacientů vyšetřovaných pro akutní infekci (36–54 %) je přijímána na standardní oddělení, přičemž jeden z pěti takových pacientů vyvine sepsi v průběhu dalších 72 hodin.5 Sepse je také nejčastějším důvodem akutní deteriorace pacientů na standardních odděleních. Zmíněný český projekt EPOSS ukázal, že prognóza septických pacientů překládaných na jednotky intenzivní péče ze standardních stanic interních oddělení je významně horší (45,1 %) než prognóza pacientů přijímaných primárně z nízkoprahových příjmových oddělení (26,5 %).3 Správná a především včasná diagnóza sepse, respektive časné zahájení její léčby, je základním předpokladem pro snížení vysoké úmrtnosti, nákladů na její léčbu a zlepšení dlouhodobé kvality života pacientů. Díky své heterogenitě však sepse zůstává stále obtížně stanovitelnou diagnózou, neexistuje žádný zlatý standard či biomarker pro potvrzení její diagnózy. Vysokou variabilitu a míru subjektivity při stanovení diagnózy sepse dobře dokumentuje nedávný průzkum 94 intenzivistů z akademických center, který ukázal značné interindividuální rozdíly při hodnocení pěti fiktivních, ale klinicky velmi reálných případů sepse.6
Původní definice sepse z roku 1991 (Sepsis‑1) byla založena společně s přítomností infekce na kritériích systémové zánětlivé odpovědi (systemic inflammatory response syndrome, SIRS). Ke splnění diagnózy sepse u pacienta s infekcí dostačovala dvě ze čtyř kritérií SIRS (leukocytóza, horečka, tachykardie, tachypnoe). Podstatu definice sepse jako systémové zánětlivé odpovědi na infekci nezměnila ani aktualizace její definice z roku 2001 (Sepsis‑2), kdy byla kritéria sepse doplněna o rozsáhlý seznam dalších klinických a laboratorních odchylek, jež ještě více prohlubují nízkou specificitu diagnostických nástrojů sepse. Ve snaze odlišit závažnost sepse byla do praxe uvedena klasifikace sepse (= infekce + SIRS), těžká sepse (= infekce + SIRS + akutní dysfunkce orgánů) a septický šok (= těžká sepse + hypotenze nereagující na tekutinovou resuscitaci). Kritéria SIRS však byla opakovaně kritizována pro značný počet falešně pozitivních i falešně negativních případů sepse a pro přílišný důraz na koncept nadměrné zánětlivé odpovědi. Přítomnost kritérií SIRS v průběhu infekce velmi často představuje zcela fyziologickou, tj. žádoucí odpověď imunitního systému na nezávažnou infekci. Dnes je navíc známo, že zejména u starší populace nemocných s řadou komorbidit nebo u imunosuprimovaných pacientů probíhá sepse i při minimální aktivaci proinflamatorních procesů a na patogenezi orgánové dysfunkce způsobené sepsí se podílí řada dalších mechanismů (metabolické, bioenergetické, antiinflamatorní, hormonální apod.). Přeneseno do klinické praxe, řada nemocných s infekcí nesplní žádné z kritérií SIRS, přesto jejich stav může být komplikován rozvojem sepse nebo septického šoku (typicky pacient v dialyzační péči). Literární data ukazují, že jeden z osmi pacientů s diagnózou sepse a současné akutní orgánové dysfunkce nesplňuje ani dvě ze čtyř kritérií SIRS.7 V neposlední řadě původní pojetí sepse, založené na kritériích SIRS, významně ovlivnilo epidemiologická data. Masivní nárůst incidence sepse společně s poklesem její mortality v posledních deseti letech je zčásti důsledkem dilučního efektu epidemiologických dat (fenomén Willa Rogerse).
S důrazem na odlišení jinak nekomplikované infekce od sepse a s cílem poskytnout nástroj k časné identifikaci pacientů s vysokým rizikem úmrtí byla v roce 2016 v Journal of American Medical Association publikována nová definice sepse označovaná též jako Sepsis‑3.8 Podkladem pro formulaci této definice byla retrospektivní analýza dat 1,3 milionu pacientů. Cílem analýzy bylo nalézt taková data, která zvýší přesnost a rychlost stanovení diagnózy sepse a umožní odlišit nekomplikovanou infekci od té, jež vede k akutní orgánové dysfunkci, a jež je tudíž spojena s významně vyšším rizikem úmrtí. Sepse je nově definována jako život ohrožující orgánová dysfunkce způsobená deregulovanou odpovědí hostitelského organismu na přítomnost infekce. Definice tudíž vyžaduje rozpoznání akutní orgánové dysfunkce. K tomuto účelu je určeno skóre Sequential/Sepsis‑related Organ Failure Assessment (SOFA).9 Pomocí bodové stupnice (0–4 body) hodnotí respirační funkce, parametry koagulace, jaterní a renální funkce, hemodynamiku a stav vědomí (např. viz https://www.mdcalc....ment‑sofa‑score). Skóre SOFA vyžaduje řadu laboratorních testů, které nemusejí být vždy včas dostupné a jsou vhodné zejména pro prostředí jednotek intenzivní péče. S cílem zjednodušit a zrychlit posouzení přítomnosti orgánové dysfunkce způsobené sepsí v přednemocniční péči, na urgentních příjmech a standardních odděleních doporučuje nová definice používat tzv. qSOFA (quickSOFA). Jde o tříbodový systém, kde každý bod reprezentuje odchylku v jednom vitálním parametru: nízký krevní tlak (systolický krevní tlak [STK] ≤ 100 mm Hg), tachypnoe (≥ 22 dechů za minutu), změna vědomí (Glasgow Coma Scale < 15). Přítomnost dvou nebo více bodů qSOFA u pacienta s infekcí znamená vysokou pravděpodobnost sepse a významně vyšší riziko nepříznivého průběhu akutního onemocnění a je indikací k aktivnímu pátrání po dalších projevech akutní orgánové dysfunkce. Septickým šokem se nyní z pohledu nové klinické definice rozumí stav, kdy je sepse komplikována rozvojem hypotenze, která navzdory dostatečné objemové resuscitaci vyžaduje užití vazopresoru k dosažení středního arteriálního tlaku ≥ 65 mm Hg a současně je přítomna koncentrace laktátu > 2 mmol/l. Tento stav je spojen s více než 40% nemocniční mortalitou. Srovnání původních vymezení a nové definice shrnuje obr. 1. Ze srovnání plyne, že koncept SIRS může být užitečným nástrojem k rozpoznání infekce (ale pozor, není podmínkou!), nikoliv však diagnostickým kritériem sepse. Původní pojem těžká sepse nová definice již nezná, koncepčně jí v nové definici odpovídá sepse jako taková, kdy přítomnost akutní orgánové dysfunkce (jako projev deregulované odpovědi na infekci) je nyní striktním požadavkem pro stanovení její diagnózy.
Jak pracovat s novou definicí aneb sepse jako „medical emergency“
Nová definice sepse je velmi jednoduchá, nepouští se do oblastí, kterým zatím současná medicína nerozumí. Sepsis‑3 umožňuje vzbudit podezření na sepsi i u pacientů, kde diagnóza infekce není klinicky jednoznačná, ale nově vzniklá a jinými příčinami nevysvětlitelná porucha funkce klíčových orgánových systémů nutí na nepoznanou infekci v rámci diferenciální diagnózy myslet (např. dialyzovaný pacient s akutní změnou stavu vědomí či hypotenzí). Silný statisticky prokázaný vztah mezi infekcí provázenou akutní orgánovou dysfunkcí a mortalitou vrací pojmu sepse potřebný respekt (na rozdíl od infekce se současnou leukocytózou a tachykardií, které stačily k definici sepse) a pro kliniky hovoří zcela srozumitelným jazykem. Je imperativem urgentnosti, nutí sepsi vnímat jako skutečnou „medical emergency“, tedy stav, který zasluhuje neodkladné zahájení diagnostického a terapeutického vedení léčby (základní trias: antimikrobiální léčba, kontrola zdroje infekce, tekutinová léčba), včetně rozvahy o dalším směrování pacienta (JIP versus standardní oddělení). Na rozdíl od původní definice klade Sepsis‑3 důraz na identifikaci pacientů s vysokým rizikem dalšího zhoršení stavu a dává k tomu základní nástroj – qSOFA. Vyhodnocení tří komponent qSOFA (vědomí, dechová frekvence, krevní tlak) je dostupné během jedné až dvou minut klinického vyšetření s možností opakované reevaluace aktuálního stavu přímo u lůžka nemocného na standardním oddělení či na příjmové ambulanci.
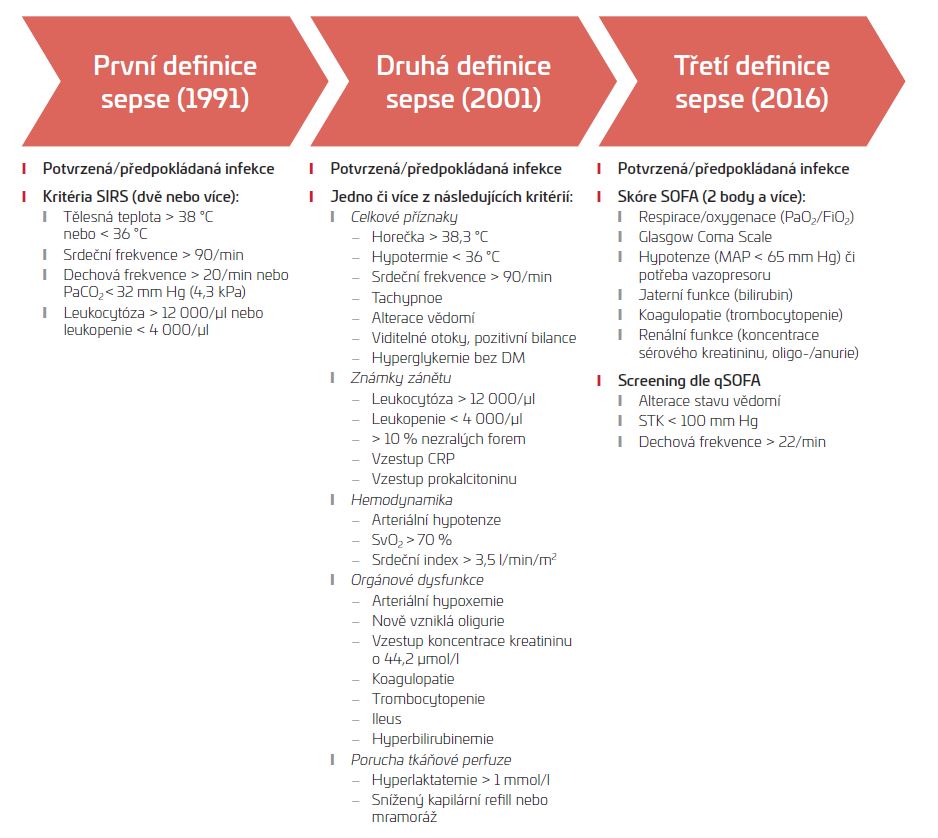
OBR. 1 Srovnání původních definic a nové definice sepse
CRP – C‑reaktivní protein; DM – diabetes mellitus; FiO2 – inspirační koncentrace kyslíku; MAP – střední arteriální tlak; PaCO2 – parciální tlak oxidu uhličitého
v arteriální krvi; PaO2 – parciální tlak kyslíku v arteriální krvi; SIRS – kritéria systémové zánětlivé odpovědi (systemic inflammatory response syndrome); SvO2 – saturace smíšené žilní krve; STK – systolický krevní tlak.
Definice Sepsis‑3 tak poskytuje klinicky užitečný koncepční rámec především pro méně zkušené lékaře či segment zdravotní péče, jakými jsou oddělení neselektovaného příjmu, přednemocniční péče či standardní oddělení. Pro tyto oblasti jednoduchá definice a klinická kritéria sepse a septického šoku zdůrazňují tři stěžejní kroky při rutinním vyhodnocení a léčbě pacienta s podezřením na infekci: 1) stanovení diagnózy infekce a její včasná léčba (zahrnuje odběry k mikrobiologickému vyšetření včetně hemokultur a včasné podání vhodných antibiotik), 2) aktivní posouzení akutní orgánové dysfunkce k rychlé stratifikaci rizika pacienta a pojmenování stavu jako „sepse“, 3) rozpoznání a léčbu hypotenze jako jednoho z klíčových určovatelů prognózy pacientů s infekcí (podání vyvážených krystaloidních roztoků a bezprostřední vyhodnocení jejich účinku, konzultace intenzivisty).
Sepse v klinické praxi není fenoménem „vše, nebo nic“. Je nutné počítat se značně rozsáhlou „šedou zónou“ v jejím rozpoznání. Budeme nadále konfrontováni s významnou subpopulací pacientů, na kterou nebude pasovat žádná z definic sepse, přesto tímto syndromem budou trpět. Budou to především pacienti, u kterých je sepse komplikací jiného či jiných závažných akutních či chronických stavů. Podobně jako absence kritérií SIRS, ani nesplnění kritérií qSOFA nevylučuje sepsi (např. pacient s infekcí a současnou trombopenií a akutním poškozením ledvin), a naopak jejich přítomnost není jejím absolutním synonymem navzdory současně přítomné infekci (např. ovlivnění kvality vědomí medikací, v perioperačním období, chronickým kognitivním deficitem, tachypnoe způsobená anxietou, bolestí, exacerbací chronické obstrukční plicní nemoci). Axiomem pro praxi zůstává, že pokud vznikne důvodné klinické podezření na rozvoj sepse (pacient „vypadá nemocně“ nebo „se neočekávaně náhle zhorší“ a nemáme pro to jiné vysvětlení), je třeba vždy postupovat bez ohledu na naplnění či nenaplnění diagnostických kritérií (ať ve smyslu qSOFA, či původního konceptu SIRS). Stejně tak nesplnění kritérií v rámci qSOFA nemůže pacienta s předpokládanou či potvrzenou infekcí automaticky vylučovat z úvah o rizikovosti a přínosu z léčby na jednotce intenzivní péče.
Lze usuzovat, že pro zkušeného lékaře a zejména pro lékaře na jednotkách intenzivní péče nebude nový koncept představovat žádnou zásadní změnu v klinickém rozhodování a postupu. Časné rozpoznání sepse a posouzení její závažnosti zůstane pro erudovaného klinika i nadále záležitostí podvědomé aplikace bayesovského modelu – hypotéza H platí, tj. pacient má pravděpodobně sepsi, pokud pozorujeme evidenci E, tj. soubor klinických a komplementárních dat. Součástí takového souboru je simultánní vyhodnocení řady základních klinických informací – vitálních funkcí, přítomnosti a míry systémové zánětlivé odpovědi (biomarkery zánětu a infekce, např. jinou váhu bude mít informace o CRP 500 mg/l s leukocytózou 35 × 109/l ve srovnání s CRP 50 mg/l a leukocytózou 12 × 109/l), pečlivé zhodnocení ukazatelů hemodynamiky, orgánové dysfunkce a tkáňové perfuze.
Technologiemi odsouvané pečlivé klinické vyšetření („head‑to‑toe“), využívající naše základní smysly, nadále zůstává zcela zásadním pro vyhodnocení rizika septického pacienta. Periferní tkáně, například kůže, jsou mezi prvními, kde lze klinicky zaznamenat projevy alterované hemodynamiky a tkáňové perfuze u těžkých infekcí. Tři jednoduché a za každé situace vyhodnotitelné varovné známky zahrnují: 1) Výskyt skvrnitých změn barvy kůže (mramoráž) přítomných typicky v oblasti kolen, případně prstů a uší. Jednoduché skóre od 0 do 5 dle velikosti postižené oblasti od kolen směrem do periferie úzce koreluje s mortalitou, nezávisle na systémové hemodynamice.10 Vysoké skóre po šesti hodinách od úvodní hemodynamické resuscitace je silným prediktorem čtrnáctidenní mortality.10 2) Opožděný kapilární návrat, tj. rychlost obnovy prokrvení nehtového lůžka po jeho pětisekundovém stlačení. Jeho prodloužení (uniformní validovaná časová definice chybí, uvádí se hraniční hodnota 2,5–4,5 sekundy) u obecné populace akutně nemocných koreluje se závažností orgánové dysfunkce, predikuje mortalitu, a naopak jeho normalizace je spojena s lepším přežitím.11 3) Teplotní rozdíl mezi předloktím a prsty („chladná akra“), ať již subjektivně posouzený, či exaktně změřený. Rozdíl větší než 4 °C je známkou významné periferní vazokonstrikce.12
Kromě vyhodnocení vitálních funkcí, hemodynamiky a posouzení periferní perfuze je třetím důležitým krokem vyšetření koncentrace laktátu. Laktát má u septických stavů stejnou důležitost jako vysoce senzitivní troponin u akutních koronárních syndromů. Je klíčovým markerem metabolického buněčného stresu. Jeho normální koncentrace jsou s určitou nadsázkou relativní zárukou fyziologické rezervy. Naopak i mírně zvýšená koncentrace laktátu (2,1–3,9 mmol/l) je spojena s vyšší mortalitou, přičemž riziko úmrtí strmě stoupá při koncentracích laktátu > 4 mmol/l. Vyšetření laktátu má význam nejen u hypotenzních pacientů, kde zvýšené hodnoty po úvodní tekutinové resuscitaci potvrzují rozvoj septického šoku („overt shock“). Mimořádný přínos má jeho stanovení u další podskupiny septických pacientů s vysokým rizikem nepříznivého průběhu, u tzv. okultního či utajeného šoku. Jde o fenotyp sepse charakterizovaný normálním krevním tlakem, u něhož nemusejí být přítomny ani jiné známky akutní orgánové dysfunkce či klinické projevy šoku. Pamatujme, že septický pacient může být „nemocnější“, než v danou chvíli vypadá. Tato situace nastává téměř u poloviny septických pacientů, kteří nemají STK < 90 mm Hg. Zvýšené koncentrace laktátu u jinak normotenzních pacientů společně s hypertermií představují silné prediktory časného (do 72 hodin) rozvoje septického šoku navzdory účinné a včasné antibiotické léčbě.13,14 Tato podskupina nemocných vyžaduje velmi pečlivé vyhodnocení, nejlépe ve spolupráci s intenzivistou. Pokud se z jakéhokoliv důvodu (dobře v dokumentaci uvedeného) rozhodneme takového pacienta přijmout na standardní oddělení, je nezbytné zajistit jeho pečlivé sledování a časné časté zhodnocení vlivu poskytované léčby. Existuje i skupina pacientů, kteří mají perzistující hypotenzi a zcela normální koncentrace laktátu. Bylo by však chybou z uvedených informací vyvodit závěr, že se nejedná o emergentní situaci, jež nevyžaduje proaktivní přístup. Tato skupina má sice lepší prognózu, ale riziko nepříznivého průběhu stále existuje. Užitečnou může být informace, že pro stanovení koncentrace laktátu dobře poslouží i venózní krev. Vhodné je laktát odebírat po zaškrcení končetiny jako první, ale obecně krátké zaškrcení neovlivňuje výsledek. Vzhledem k dostupnosti POCT analyzátorů krevních plynů na urgentních příjmech je výsledek k dispozici během minut.
Izolované hodnocení jakéhokoliv klinického či laboratorního ukazatele není dostatečně senzitivním ani specifickým nástrojem k definitivnímu posouzení tkáňové perfuze. V multimodálním pojetí jde však o jednoduché, opakovaně snadno vyhodnotitelné a významné varovné známky, které umožňují ve většině případů rychlou triáž jakéhokoliv pacienta s akutním zhoršením stavu. Podobně jejich vývoj po úvodní intervenci je důležitým signálem úspěšnosti/neúspěšnosti přijatých léčebných opatření. Nicméně i pacient s rezolucí varovných známek v reakci na úvodní léčbu zasluhuje častou reevaluaci během prvních 48 hodin hospitalizace.
Klíčové body na závěr:
- Sepse je hlavní příčinou úmrtí na infekční choroby.
- Sepsi je nutné vnímat jako „medical emergency“, tedy stav, který vyžaduje neodkladné zahájení diagnostického a terapeutického vedení léčby, včetně rozvahy o dalším směrování pacienta.
- Sepse je nově definována jako život ohrožující orgánová dysfunkce způsobená deregulovanou odpovědí hostitelského organismu na přítomnost infekce.
- Nová definice neznamená změnu v doporučených léčebných postupech.
- Pamatujme, že septický pacient může být „nemocnější“, než v danou chvíli vypadá.
- Důvodné klinické podezření na rozvoj sepse (pacient „vypadá nemocně“ nebo „se neočekávaně náhle zhorší“ a nemáme pro to jiné vysvětlení) opravňuje k aktivním krokům bez ohledu na naplnění či nenaplnění kritérií definice.
- Sepsis‑3 = tři základní kroky zahrnující 1) stanovení diagnózy infekce, včetně její včasné léčby; 2) posouzení akutní orgánové dysfunkce k rychlé stratifikaci rizika pacienta; 3) rozpoznání a bezprostřední léčbu hypotenze.
- Při rozvoji nově vzniklé poruchy orgánových funkcí vždy zvážit infekci jako možnou příčinu zhoršení klinického stavu.
- Vyhodnocení qSOFA společně s klinickými známkami periferní hypoperfuze a stanovením koncentrace laktátu představuje základní úvodní nástroj pro bezpečnou triáž pacientů s podezřením na sepsi.
- Podceňovanou proměnou v úvodním vyhodnocení pacienta je hypotenze. Pozdní korekce hypotenze je silným nezávislým faktorem mortality.
- Pacient s přítomností uvedených „red flags“ vyžaduje aktivaci procesu/systému: příjmový lékař → intenzivista, lékař standardního oddělení → intenzivista
Literatura
- Goto T, Yoshida K, Tsugawa Y, et al. Infectious Disease Related Emergency Department Visits of Elderly Adults in the United States, 2011–2012. J Am Geriatr Soc 2016;64:31–36.
- Fleischmann C, Scherag A, Adhikari NK, et al. Assessment of Global Incidence and Mortality of Hospital treated Sepsis. Current Estimates and Limitations. Am J Respir Crit Care Med 2015;193:1–61.
- Uvizl R, Adamus M, Cerny V, et al. Patient survival, predictive factors and disease course of severe sepsis in Czech intensive care units: A multicentre, retro-spective, observational study. Biomed Pap Med Fac Univ Palacky Olomouc Czech Repub 2016;160:287–297.
- Liu V, Escobar GJ, Greene JD, et al. Hospital deaths in patients with sepsis from 2 independent cohorts. JAMA 2014;312:90–92.
- Glickman SW, Cairns CB, Otero RM, et al. Disease progression in hemodynamically stable patients presenting to the emergency department with sepsis. Acad Emerg Med 2010;17:383–390.
- Rhee C, Kadri SS, Danner RL, et al. Diagnosing sepsis is subjective and highly variable: a survey of intensivists using case vignettes. Crit Care 2016;20:89.
- Kaukonen KM, Bailey M, Pilcher D, et al. Systemic inflammatory response syndrome criteria in defining severe sepsis. N Engl J Med 2015;372:1629–1638.
- Singer M, Deutschman CS, Seymour, CW, et al. The Third International Consensus Definitions for Sepsis and Septic Shock (Sepsis 3). JAMA 2016;315:801–810.
- Vincent JL, de Mendonça A, Cantraine F, et al. Use of the SOFA score to assess the incidence of organ dysfunction/failure in intensive care units: results of a multicenter, prospective study. Working group on “sepsis related problems” of the European Society of Intensive Care Medicine. Crit Care Med 1998;26:1793–1800.
- Ait Oufella H, Joffre J, Boelle PY, et al. Knee area tissue oxygen saturation is predictive of 14 day mortality in septic shock. Intensive Care Med 2012;38:976–983.
- Ait Oufella H, Bige N, Boelle PY, et al. Capillary refill time exploration during septic shock. Intensive Care Med 2014;40:958–964.
- Lima A, Jansen TC, van Bommel J, et al. The prognostic value of the subjective assessment of peripheral perfusion in critically ill patients. Crit Care Med 2009;37:934–938.
- Casserly B, Phillips GS, Schorr C, et al. Lactate measurements in sepsis induced tissue hypoperfusion: results from the Surviving Sepsis Campaign database. Crit Care Med 2015;43:567–573.
- Glickman SW, Cairns CB, Otero RM, et al. Disease progression in hemodynamically stable patients presenting to the emergency department with sepsis. Acad Emerg Med 2010;17:383–390.
- Kategorie: Přehledové články
- Klíčová slova: sepse