Pacientka s IgA nefropatií a těžkou, pravděpodobně sekundární arteriální hypertenzí
Pacientce, 36leté ženě, byl v listopadu 2001 u praktického lékaře naměřen krevní tlak 200/110 mm Hg. Pacientka trpěla v posledních dvou letech občasnými bolestmi hlavy – TK ale v tomto období měřen nebyl. Byla zahájena antihypertenzní terapie: Prestarium 4 mg ½‑0‑0, Atenolol 25 mg 1‑0‑0. Pacientka užívala na hypertenzi přechodně také homeopatika. V listopadu 2002 byla hospitalizována na spádovém interním oddělení pro akceleraci hypertenze, bolesti hlavy a zvracení.
V rodinné anamnéze byl zajímavý údaj o otci pacientky, který měl arteriální hypertenzi od svých 25 let, dysplazii jedné ledviny a byl operován pro nefrolitiázu. Pacientka byla vdaná, měla dvě zdravé děti, byla nekuřačka.
V objektivním nálezu byl zjištěn TK 190/90 mm Hg, jinak bylo fyzikální vyšetření normální: BMI 22,1, diuréza 1 750 ml, GF 0,51 ml/s, proteinurie 3,79 g/l, U‑leu 5–10, kultivace moči negativní, urea 12,7 mmol/l, kreatinin 361 μmol/l, kyselina močová 554 μmol/l, celkový cholesterol 6,66 mmol/l, LDL 4,68 mmol/l, celková bílkovina 56 g/l, albumin 33,6 g/l. Krevní obraz, mineralogram, CRP, glykémie, bilirubin; ALT; AST; GGT; ALP, štítná žláza, EKG – v normě.
Sonograficky byly ledviny normální velikosti s normální šíří kůry, nespecifické strukturální změny parenchymu bilaterálně, steatóza jater. Echokardiografie odhalila koncentrickou hypertrofii LK; zsLK 13 mm, EF 62 % s normální diastolickou funkcí. Oční pozadí beze změn. Doporučená medikace: Prestarium 4 mg 1‑0‑0, Atenolol 25 mg 1‑0‑0, Furon 40 mg ½‑0‑0.
Pacientka byla doporučena na nefrologické pracoviště, kde byla provedena biopsie ledvin s nálezem difuzní mesangioproliferativní IgA nefropatie s významnými hypertonickými vaskulárními změnami a s výraznou atrofií parenchymu.
Nemocná setrvávala velmi dlouhou dobu v negativním postoji k zahájení dialýzy, ačkoli byla opakovaně poučena o rizikách tohoto rozhodnutí. V transplantačním centru proběhlo vyšetření k preemptivní transplantaci ledvin, ke zvážení příbuzenské transplantace, ale vhodný dárce nebyl nalezen.
V srpnu 2005 byla pacientka v terminální fázi chronického onemocnění ledvin. Měla chronickou hyperkalémii (5,6 mmol/l), kompenzovanou metabolickou acidózu, hyperfosfatémii (2,23 mmol/l) a progredující sekundární hyperparatyreózu, renální anémii (Hb 94 g/l) – zahájena léčba ESA.
Jako metoda náhrady funkce ledvin zvolena peritoneální dialýza, pacientka byla zařazena do čekací listiny na transplantaci ledviny. Pacientka podepsala negativní revers k zahájení dialyzační léčby z estetických důvodů – odpor k a.v. fistuli na předloktí, odpor k peritoneálnímu katétru vyúsťujícímu v podbřišku. Se zahájením peritoneální dialýzy souhlasila až v říjnu 2005, kdy měla s‑K 6,0 mmol/l, s‑ureu 26,4 mmol/l, s‑kreatinin 1 017 μmol/l (obr. 1).
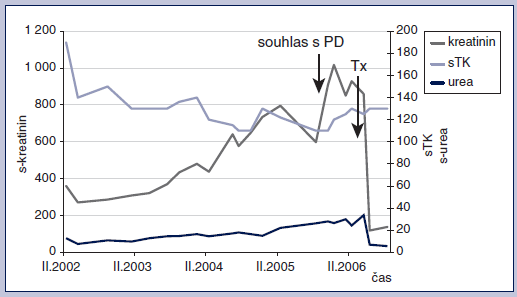
Obr. 1 Vývoj parametrů - systolického TK a sérových koncentrací kreatininu a urey - v čase. Šipkami je označena doba, kdy pacientka souhlasila se zahájením peritoneální dialýzy, a doba provedení transplantace ledviny.
Z estetických důvodů byl katétr vyveden atypicky. Tenckoffův stočený peritoneální katétr 62 cm byl subkutánně prodloužen pomocí titanové spojky a druhého katétru a vyveden dlouhým podkožním tunelem k vyústění na pravém boku ve střední axilární čáře (obr. 2). Byla zahájena peritoneální dialýza bez komplikací.
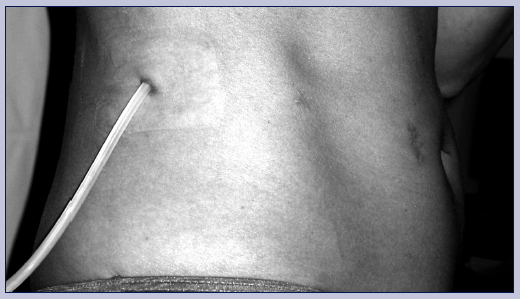
Obr. 2 Vyústění peritoneálního katétru v pravostranné střední axilární čáře. V pravé části obrázku laterálně od pupku je patrno místo (jizva), kde jsou v podkoží titanovou spojkou napojeny dvě části katétru.
V květnu 2006 proběhla transplantace kadaverózní ledviny s dobrým rozvojem funkce štěpu, sérová koncentrace kreatininu klesla na 120 μmol/l. Pacientka byla léčena trojkombinací imunosupresiv: tacrolimus, mykofenoát mofetil, prednison.
Komentář
- MUDr. Martin Havrda, I. interní klinika 3. LF UK a FNKV, Praha
Literatura
- Floege J. The pathogenesis of IgA nephropathy: what is new and how does it change therapeutic approaches? Am J Kidney Dis 2011;58:992–1004.
- Floege J, Eitner F. Current therapy of IgA nephropathy. J Am Soc Nephrol 2011;22: 1785–1794.
- Herzenberg AM, et al. Validation of the Oxford classification of IgA nephropathy. Kidney Int 2011;80:310–317.
- Le WB, et al. Long‑term renal survival and related risk factors in patients with IgA nephropathy: results from a cohort of 1155 cases in a Chinese adult population. Nephrol Dial Transplant 2011, Advance Access, Sept 29.
- Maixnerova D, et al. The retrospective analysis of 343 Czech patients with IgA nephropathy – one center experience. Nephrol Dial Transplant 2011, Advance Access, Sept 2.
- Kategorie: Kazuistiky
- Klíčová slova: hypertenze (vysoký krevní tlak); kazuistika; nefropatie
IgA nefropatie je nejčastější typ primární glomerulonefritidy v rozvinutých zemích. Jejím charakteristickým znakem jsou depozita imunokomplexů obsahujících imunoglobuliny IgA, která se nacházejí zejména v mesangiu. Přítomnost těchto depozit je v sekčních nálezech nebo v ledvinách určených k transplantaci velmi častá (5–20 %) a u většiny osob není spojena s klinicky zjevným onemocněním.
Průběh „symptomatické“ IgA nefropatie je velmi různorodý, z čistě klinického hlediska často němý a pokud hovoříme o symptomech, máme na mysli převážně známky laboratorní. Typickým projevem je mikroskopická nebo makroskopická hematurie. Proteinurie nemusí být přítomna vůbec, často je mírná, ale může se vyvinout i typický nefrotický syndrom. Z hlediska dopadu na renální funkci může být onemocnění zcela benigní, asi u 30 % diagnostikovaných případů nastává pozvolná progrese v průběhu deseti i více let, která může vyústit do terminálního selhání ledvin. U malé části nemocných choroba probíhá agresivněji, a to i pod obrazem rychle progredující glomerulonefritidy. Na přítomnost onemocnění mohou nemocného upozornit makroskopická hematurie, otoky při nefrotickém syndromu, příznaky arteriální hypertenze (například bolesti hlavy), případně až projevy poruchy funkce ledvin či jejich selhání.
Z patogenetického hlediska hraje u IgA nefropatie roli abnormální galaktosylace molekul imunoglobulinu IgA1, produkce protilátek IgG proti těmto molekulám, mesangiální depozice nebo formování imunokomplexů tvořených na bázi těchto molekul, aktivace mesangiálních receptorů pro IgA nebo komplementu, poškození mesangiálních buněk a aktivace sekundárních mechanismů, vedoucích ke glomeruloskleróze a k tubulointersticiální fibróze.
Hodnocení prognózy nemocných s IgA nefropatií je založeno na klinických a patologických kritériích. Z klinického hlediska má prognostický význam proteinurie > 0,5–2 g/24 h, zejména pokud trvá v průběhu sledování, dále snížení glomerulární filtrace na < 1 ml/s v okamžiku diagnózy, přítomnost arteriální hypertenze, hypoproteinémie a hyperurikémie. Z histologického hlediska byly jako prediktory renální prognózy identifikovány zejména podíl glomerulů se segmentální sklerózou, adhezemi nebo endokapilární proliferací, procento tubulární atrofie a intersticiální fibrózy. Významnou roli ovlivňující aktivitu onemocnění hrají zánětlivá a infekční onemocnění. U části nemocných dochází ke spontánní remisi. Pomocí rebiopsií bylo prokázáno, že může dojít k vymizení depozit.
Z praktického hlediska dělíme nemocné na ty, kteří mají nízké riziko progrese – s malým močovým nálezem (typicky izolovaná hematurie), s normální glomerulární filtrací, bez hypertenze, a na ty, kteří mají střední nebo vyšší riziko progrese – s proteinurií > 0,5–1,0 g/24 h, se sníženou glomerulární filtrací, s hypertenzí. Zvláště závažný nález představuje rychle klesající glomerulární filtrace.
Léčba IgA nefropatie je založena zejména na těsné kontrole krevního tlaku, na podávání látek inhibujících systém renin‑angiotensin‑aldosteron, na restrikci příjmu bílkovin a na dalších, tzv. nefroprotektivních léčebných postupech. Léčba rybím olejem se podle některých studií jevila nadějná, ale metaanalýzou nebyl její efekt prokázán. Účinnost antiagregační a antikoagulační léčby nebyla spolehlivě prokázána. Pokud jsou vzplanutí IgA nefropatie indukována recidivujícími tonsilitidami, doporučuje se provedení tonsilektomie, ale význam tohoto výkonu obecně u IgA nefropatie nebyl dostatečně prokázán. Význam kortikoterapie podávané po dobu šesti měsíců byl prokázán zejména u nemocných s proteinurií a nepříliš sníženou glomerulární filtrací (GF > 0,8 ml/s). Léčba vedla k poklesu proteinurie a k lepšímu zachování funkce ledvin. Význam jiných imunosupresiv nebo jejich kombinací (cyklofosfamid, azathioprin, mykofenolát mofetil, případně s kortikoidy) je sporný. Je nutno připomenout, že uspořádání validní kontrolované klinické studie léčby IgA nefropatie je ztíženo heterogenitou onemocnění a zpravidla malými počty pacientů. Proto není léčba tohoto onemocnění zcela jednotná a často probíhá podle místních léčebných protokolů nefrologických pracovišť. U nemocných, u nichž onemocnění probíhá pod obrazem rychle progredující glomerulonefritidy klinicky (rychlý pokles glomerulární filtrace) i histologicky (čerstvé srpky), je obvykle volena léčba kombinací cyklofosfamidu a kortikoidů. U nemocných s významně sníženou glomerulární filtrací, zejména převažují‑li histologicky sklerotické změny, bývá indikována pouze nefroprotektivní léčba.
Kasuistika demonstruje případ pacientky, u níž se IgA nefropatie rozvíjela plíživě a vedla poměrně brzy k selhání ledvin. Tento nepříznivý vývoj by pravděpodobně bylo možné zbrzdit, případně zvrátit, pokud by bylo onemocnění diagnostikováno včas a správně léčeno. Zde vidíme spíše liknavost diagnostického a léčebného postupu a některá nesprávná rozhodnutí. Prvním příznakem onemocnění byla nově vzniklá cefalea způsobená pravděpodobně sekundární hypertenzí, která byla diagnostikována se zpožděním nejméně dvou let. Správně by měl být každý pacient s nově vzniklými bolestmi hlavy důkladně vyšetřen a pátrání po arteriální hypertenzi se u nemocné, jejíž otec navíc rovněž trpí hypertenzí, je nasnadě. Když byla arteriální hypertenze konečně diagnostikována, nebyla zřejmě provedena žádná vyšetření ke zjištění její příčiny. Správně by taková vyšetření měla být provedena, zvláště když se jednalo o nově vzniklou těžkou hypertenzi u mladé ženy. Byla zahájena léčba malou dávkou inhibitoru ACE a malou dávkou beta‑blokátoru, která pravděpodobně nebyla dostatečně účinná. Z dnešního, ale ani tehdejšího hlediska nelze tuto léčbu považovat za optimální. Inhibitor ACE je pro tuto pacientku vhodný (pokud je zajištěna antikoncepce), dávka perindoprilu 2 mg denně je však (s výjimkou samotného zahájení léčby) nepřiměřeně nízká. Beta‑blokátor není v tomto případě do úvodní linie léčby vhodný, není‑li pro něj jasná indikace, např. srdeční selhání nebo tachykardie. Použitá dávka je navíc z indikace hypertenze velmi nízká. Další vývoj ukázal, že aplikovaná léčba byla zcela nedostatečná.
Hospitalizace pro akcelerovanou arteriální hypertenzi přivedla nemocnou na nefrologické pracoviště, kde byla biopticky diagnostikována IgA nefropatie. V okamžiku diagnózy již měla pacientka všechny rizikové faktory rychlé progrese onemocnění – sníženou glomerulární filtraci, arteriální hypertenzi, proteinurii přesahující 1 g/24 h a histologický průkaz výrazných tubulointersticiálních změn s atrofií renálního parenchymu. Byla indikována nefroprotektivní léčba, o níž je prokázáno, že zpomaluje progresi do selhání ledvin. Šlo o těsnou kontrolu hypertenze a podávání inhibitorů ACE. Kortikoterapie ani jiná forma imunosupresivní terapie nebyla indikována vzhledem k bioptickému nálezu, kde dominovala atrofie parenchymu a vaskulární změny, nikoli aktivní zánětlivé změny. K rozvoji selhání ledvin došlo během čtyř let od diagnózy.
Tato kasuistika poukazuje na velký význam arteriální hypertenze jako faktoru urychlujícího progresi nefropatií. U nemocných s IgA nefropatií a těžkou arteriální hypertenzí pravidelně pozorujeme rychlou progresi poruchy funkce ledvin. Včasná diagnostika a adekvátní léčba může vývoj onemocnění zpomalit, nebo i odvrátit rozvoj selhání ledvin.