Hluboká žilní trombóza jako primární manifestace COVID 19 u pacienta po transplantaci ledviny
Úvod
Představujeme kazuistiku pacienta referovaného pro hlubokou žilní trombózu na straně transplantované ledviny. Z tohoto důvodu bylo urgentně žádáno vyšetření pacienta v transplantačním centru. V rámci vyšetření byla při příjmu zjištěna pozitivita COVID‑19.
Naším pacientem je 35letý muž se selháním ledvin na podkladě IgA nefropatie, tři roky po příbuzenské transplantaci ledviny, léčený udržovací imunosupresí takrolimem, sirolimem, prednisonem. Vzhledem ke dva dny trvajícímu bolestivému otoku pravého stehna byl vyšetřen na urgentním příjmu s potvrzením femoropopliteální trombózy. Přestože u něj byla prokázána mutace faktoru V Leiden v heterozygotní formě, jednalo se u tohoto pacienta o první klinickou manifestaci trombofilního stavu.
V recentní anamnéze nebyly přítomny jiné rizikové faktory tromboembolické nemoci. Teoreticky můžeme zvažovat podíl venostázy při uložení štěpu v pravé jámě kyčelní. Vzhledem k tomu, že sonograficky nebylo spolehlivě možné diferencovat čelo trombu, byl pacient k vyloučení trombózy štěpu při zhoršené renální funkci akutně referován na naše pracoviště. Jednalo by se o závažnou komplikaci, která by mohla vést ke ztrátě funkce transplantovaného orgánu.
Pacient byl u nás vstupně subfebrilní, normotenzní, normosaturovaný, při vyšetření dominovala pouze bolestivost oteklé pravé dolní končetiny a diskrétní poslechový nález. Ze subjektivních obtíží uváděl občasný suchý kašel‚ který byl dle pacienta přítomen již rok po prodělané pneumonii.
Laboratorně byla zjištěna zhoršená renální funkce z chronických hodnot sérového kreatininu (S‑Cr) 160 µmol/l na aktuální S‑Cr 210 µmol/l a zvýšené D‑dimery v hodnotě 8 560 µg/l. Jinak byly laboratorní nálezy bez větších pozoruhodností, C‑reaktivní protein (CRP) 37 mg/l v rámci přítomné flebotrombózy, močový sediment bez známek zánětu. Až na chronickou tendenci k trombocytopenii (97 × 109/l) byl krevní obraz včetně diferenciálního rozpočtu leukocytů v normě, morfologicky však s reaktivními formami lymfocytů, jež se vyskytují u některých viróz. Sonograficky byl štěp ledviny s přiměřenou perfuzí, s přítomným arteriálním i žilním signálem a normálními rezistenčními indexy. Při rentgenovém vyšetření hrudníku již na spádovém pracovišti nebyly popsány patologické změny.
V rámci epidemiologických opatření byl u pacienta proveden výtěr z nosohltanu na COVID‑19 metodou polymerázové řetězové reakce (PCR) a antigenním rychlotestem, oba s pozitivním výsledkem. Zahájili jsme terapii hydrokortizonem, empiricky cefuroximem a antikoagulační léčbu nízkomolekulárním heparinem. Imunosuprese byla přechodně přerušena.
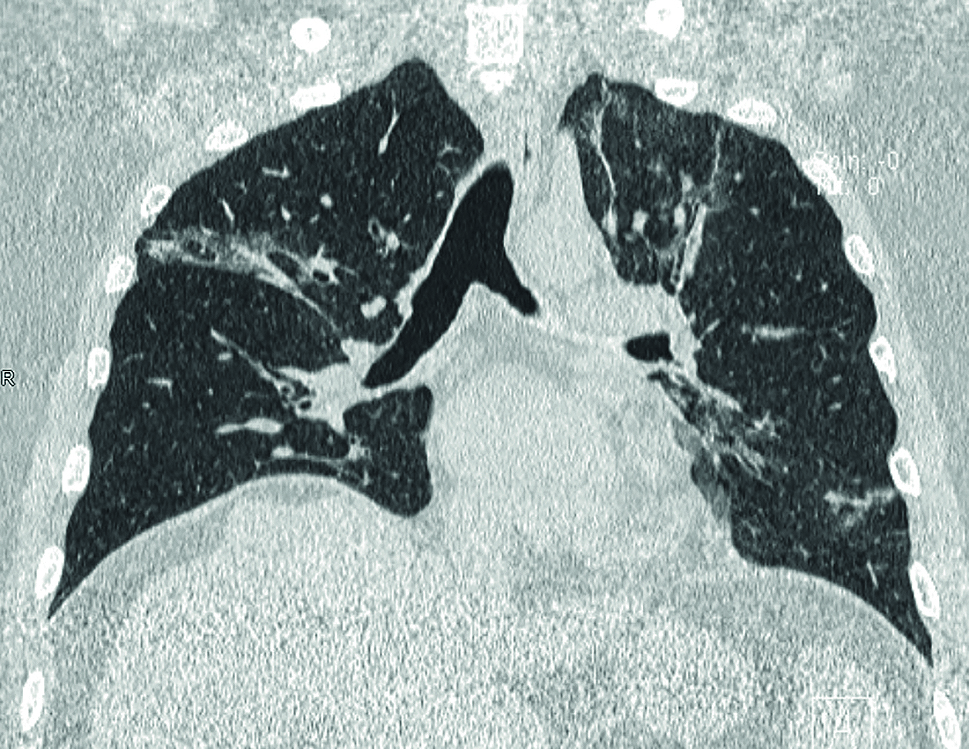
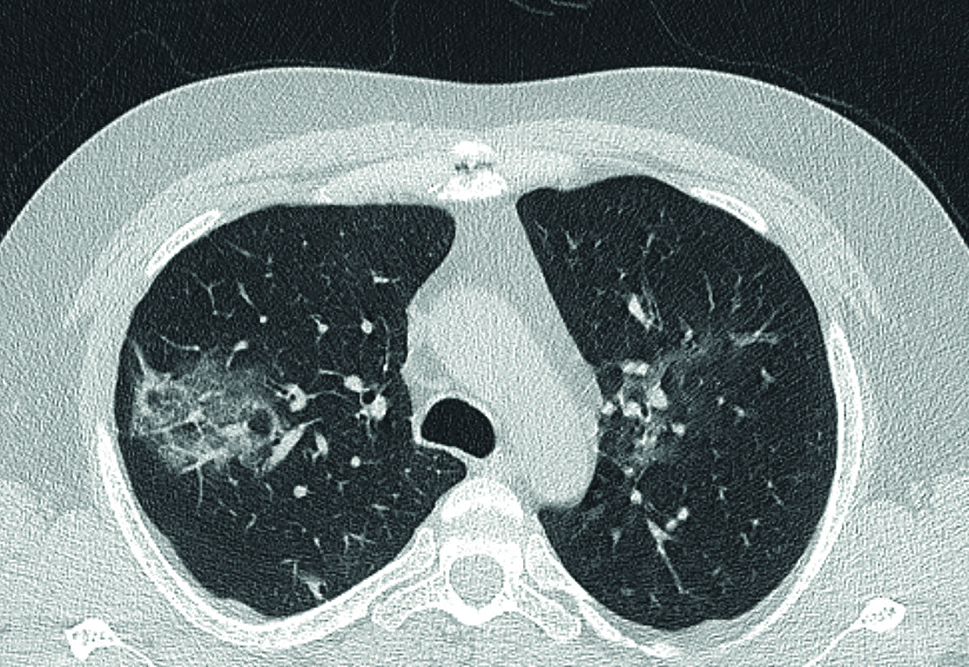
Vzhledem k tomu, že šlo o imunosuprimovaného pacienta po prodělané pneumonii v roce 2019 se závažným průběhem a nyní s manifestovaným trombofilním stavem, doplnili jsme druhý den hospitalizace výpočetní tomografii s vysokým rozlišením (HRCT) plic s nálezem oboustranných cárovitých kondenzací typu mléčného skla v plicním parenchymu (obr. 1). Dle zobrazovacích metod byl kmen plicnice bez dilatace s normálními parametry.
OBR. 1 HRCT – na snímku v koronárním a axiálním řezu nález kondenzací typu mléčného skla s predilekcí v pravé plíci (Bc. Hrdličková, Bc. Zapletal, MUDr. Šmejkal).
HRCT – výpočetní tomografie s vysokým rozlišením.
V dalším průběhu hospitalizace byla pozorována leukopenie (2,5 × 109/l) s lymfopenií s minimální hodnotou lymfocytů 0,6 × 109/l.
Vzhledem k potvrzení pneumonie na HRCT u nemocného po transplantaci jsme rozhodli o podání remdesiviru. Remdesivir jsme podali v celkem pěti dávkách: první den v úvodní dávce 200 mg i.v., druhý až pátý den v dávce 100 mg i.v. Vzhledem k renální funkci (Chronic Kidney Disease – Epidemiology Collaboration [CKD‑EPI] 34 ml/min/1,73 m2) nebyla nutná úprava dávek. Léčbu jsme doplnili podáním dvou jednotek rekonvalescentní plazmy.
Průběh hospitalizace byl nekomplikovaný. Až na intermitentní febrilie (maximum 38,4 °C) byl pacient v dobrém klinickém stavu, bez nutnosti kyslíkové podpory. Pacienta jsme devátý den propustili do domácí izolace se zavedenou účinnou antikoagulací enoxaparinem, s obnovenou renální funkcí s hodnotou S‑Cr 126 µmol/l, na dvojkombinaci imunosupresivní terapie takrolimus a prednison. Týden po dimisi v rámci ambulantní kontroly byla vzhledem k dobrému celkovému stavu změněna imunosuprese na trojkombinaci takrolimus, mykofenolová kyselina, prednison.
Komentář
Literatura
- Klok FA, Kruip MJHA, van der Meer NJM, et al. Incidence of thrombotic complications in critically ill ICU patients with COVID‑19. Thromb Res 2020;191:145–147.
- RECOVERY Collaborative Group, Horby P, Lim WS, Emberson JR, et al. Dexamethasone in Hospitalized Patients with Covid‑19 – Preliminary Report. N Engl J Med 2020 Jul 17:NEJMoa2021436. doi: 10.1056/NEJMoa2021436. Epub ahead of print. PMID: 32678530; PMCID: PMC7383595.
- http://www.sukl.cz/modules/medication/detail.php?code=0249655&tab=texts
- Beigel JH, Tomashek KM, Dodd LE, et al.; ACTT‑1 Study Group Members. Remdesivir for the Treatment of Cov&#&id‑19 – Final Report. N Engl J Med 2020;383:1813–1826.
- Adamsick ML, Gandhi RG, Bidell MR, et al. Remdesivir in Patients with Acute or Chronic Kidney Disease and COVID‑19. J Am Soc Nephrol 2020;31:13&scent‑plasma/
- Maggiore U, Abramowicz D, Crespo M, et al. How should I manage immunosuppression in a kidney transplant patient with COVID‑19? An ERA‑EDTA DESCARTES expert opinion. Nephrol Dial Transplant 2020;35:899–904
- Kategorie: Kazuistiky
- Klíčová slova: COVID-19; remdesivir; transplantace ledvin; tromboembolické komplikace
Předkládaná kazuistika velmi dobře ilustruje současnou situaci, kdy je zdravotní péče ve všech zařízeních významně komplikována šířící se infekcí COVID‑19. Kterýkoli pacient může trpět závažnou, ve chvíli vyšetření oligosymptomatickou, ale v dalším průběhu potenciálně letální a v neposlední řadě vysoce nakažlivou virovou infekcí. Takováto hrozba byla do letošního roku v českém zdravotnictví nevídaná.
Jako superkonziliární pracoviště nabízíme pomoc zejména v případech, kdy ošetřující lékař vysloví podezření na stav potenciálně hrozící ztrátou funkce transplantovaného orgánu. V tomto konkrétním případě se jednalo o trombózu dolní končetiny s nediferencovaným čelem trombu u pacienta se známou trombofilní mutací a zhoršením funkce štěpu ledviny. Zpětně můžeme hodnotit následně prokázanou infekci COVID‑19 jako suspektní bezprostřední příčinu proběhlé trombózy při absenci jiných rizikových faktorů.1
Celkovou závažnost stavu můžeme klasifikovat jako středně těžký průběh, kdy pacient vyžaduje hospitalizaci bez nutnosti oxygenoterapie, ale dle zobrazovacího vyšetření pneumonie prokázána je. V rámci léčebných opatření bylo reagováno přechodnou redukcí udržovací imunosuprese na kortikoterapii. V nedávné randomizované studii vedlo podávání dexametazonu ke zlepšení prognózy.2 Dle zvyklostí našeho pracoviště nebyl použit dexametazon, ale hydrokortizon v ekvivalentní dávce.
U pacienta byla indikována terapie remdesivirem, který již má indikaci COVID‑19 asociované pneumonie i v českém SPC.3 Výsledky z nedávno publikované studie ukazují, že remdesivir je nadějným podpůrným přípravkem, který zkracuje čas do zotavení, dobu závislosti na oxygenoterapii a slouží jako prevence závažného zhoršení stavu a potřeby intubace.4 Limitací pro nefrologii je zvýšená opatrnost u pacientů s glomerulární filtrací (GFR) <0,5 ml/s/1,73 m2. U našeho pacienta byla GFR vyšší. Nicméně i pokud by nesplňoval doporučené kritérium, je možné terapii zvážit. Obava z toxicity remdesiviru u renální insuficience je dána zejména nosičem účinné látky, což je sodná sůl sulfobutoxybetadexu, která se u renální insuficience může kumulovat a způsobit v nejhorším případě tubulární obstrukci. Stejný nosič je použit také u i.v. formy vorikonazolu, kterou je v nezbytných případech třeba použít u pacientů s invazivními mykotickými infekcemi. Renální insuficience by tedy neměla vést k úplnému odsouzení použití remdesiviru, ale k nezbytné opatrnosti a důkladnému zvážení přínosu a rizika.5
Použití mražené plazmy zatím čeká na data z prospektivních randomizovaných studií,6 přesto rekonvalescentní plazmu Úřad pro kontrolu potravin a léčiv (Food and Drug Administration, FDA) schválil v srpnu 2020 a v současnosti je s termíny „convalescent plasma/COVID‑19“ registrováno 166 studií (ClinicalTrials.gov).
Zlepšený stav pacienta umožnil rychlé vrácení imunosupresivní dvojkombinace s takrolimem a kortikoidy a následně byl při ambulantní kontrole přidán mykofenolát v redukované dávce. Pokud není dosaženo spolehlivé kontroly infekce, je doporučeno vysazení mykofenolátu.7
V současné době informace o onemocnění COVID‑19 stárnou rychleji než u jakéhokoli jiného onemocnění v historii a také je pravděpodobné, že i naše osobní zkušenost bude rychle narůstat.