Vzácný případ Goodpastureovy nemoci u batolete
Kazuistika
V našem kazuistickém sdělení popisujeme vzácný případ Goodpastureovy nemoci u dosud zdravého batolete.
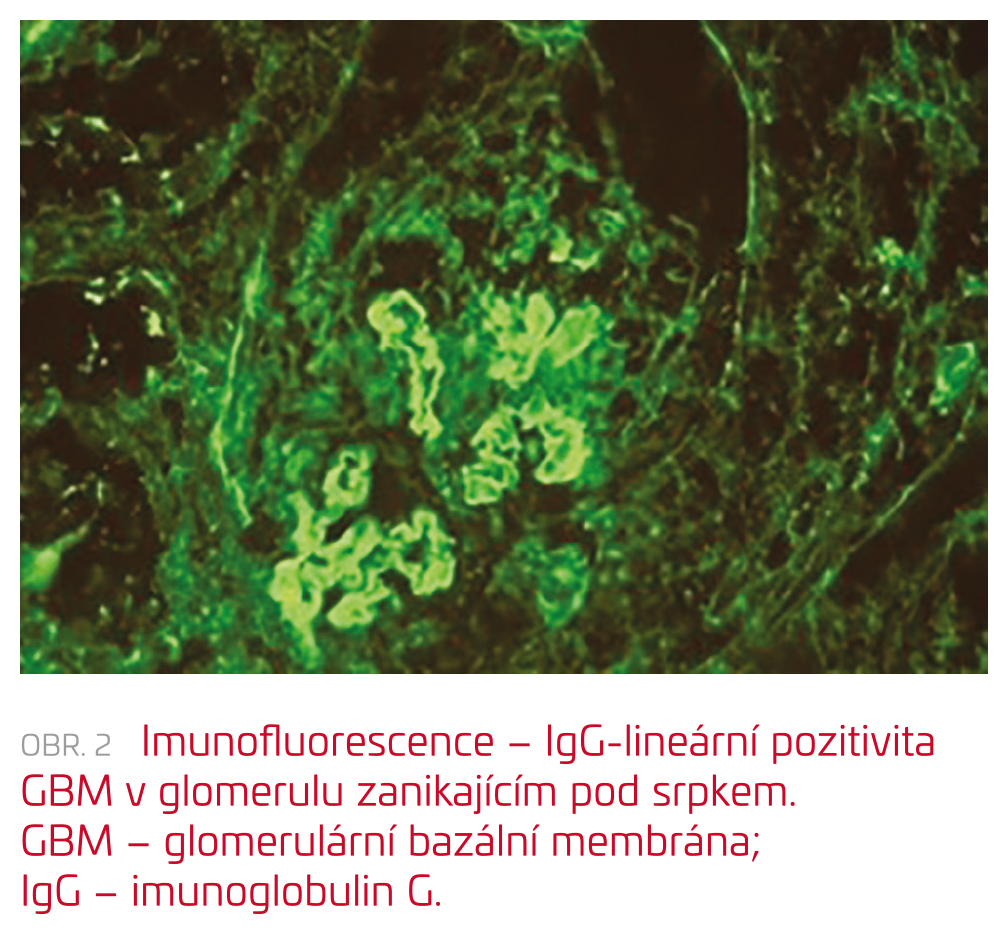
Sedmnáctiměsíční pacientka s třídenní anamnézou intermitentní makroskopické hematurie byla vyšetřena praktickým lékařem pro děti, který stav uzavřel jako akutní infekci močových cest. Nasazení perorální antibiotické léčby však nevedlo ke zlepšení klinického stavu dítěte. Dívka byla subfebrilní až febrilní, začala opakovaně zvracet a rozvinuly se u ní průjmovité stolice. Pro intoleranci perorálních antibiotik a suspekci na akutní pyelonefritidu byla pacientka přijata na pediatrické oddělení lokální nemocnice. Při přijetí byla dívka febrilní, bledá, normotenzní, byl zjištěn systolický šelest dvě šestiny nad hrotem a mírné otoky dolních končetin, diuréza byla normální. Při laboratorním vyšetření byla patrná mikrocytární anémie s tendencí k progresi, trombocytóza, snížená glomerulární filtrace, hypoalbuminemie a elevace hodnot renálních parametrů. Chemické vyšetření moči prokázalo hraniční leukocyturii a patologickou proteinurii i hematurii. Vzhledem ke zmíněným klinickým a laboratorním nálezům (tab. 1) bylo vysloveno podezření na akutní glomerulonefritidu a dívka byla přeložena na naše pracoviště.
Pro výraznou anémii jsme pacientce vstupně podali transfuzi erytrocytů. Při nálezu vysokých hodnot zánětlivých parametrů a trvání febrilií jsme pokračovali v parenterální antibiotické léčbě. V rámci diferenciální diagnostiky možné infekční příčiny obtíží byla doplněna široká mikrobiologická vyšetření s negativním nálezem: výtěr z nazofaryngu na polymerázovou řetězovou reakci (PCR) respiračních virů, výtěr z krku, z rekta, PCR ze stolice, hemokultivace, PCR virů z plné krve – virus Epsteina–Barrové (EBV), cytomegalovirus (CMV), virus herpes simplex (HSV), virus varicella zoster (VZV), lidský humánní herpetický virus (HHV6), HHV7, parvovirus B19, adenovirus, sérologie Toxoplasma gondii, sérologie Chlamydophila pneumoniae, Mycoplasma pneumoniae, brucelózy, tularemie, listeriózy, Yersinia enterocolitica, antigen rodů Candida a Aspergillus. Na ultrazvuku břicha byla popsána pouze difuzní parenchymová léze ledvin bez další patologie. Rentgen hrudníku ukázal pouze nevýrazný zánětlivý infiltrát vlevo parahilózně. Bylo doplněno základní imunologické vyšetření (imunoglobuliny, autoprotilátky: antinukleární protilátky [ANA], protilátky proti cytoplazmě neutrofilních leukocytů [ANCA], protilátky proti dvouvláknové DNA [dsDNA], protilátky proti extrahovatelnému nukleárnímu antigenu [ENA], C3 a C4 složka komplementu) – vše v normě. V moči přetrvával nález nefrotické proteinurie smíšeného rázu. Šestý den hospitalizace byla provedena renální biopsie s překvapivým nálezem – anti‑GBM floridní nekrotizující glomerulonefritidy s objemnými epitelovými srpky s rozsáhlým postižením všech glomerulů ve vzorku (obr. 1). V intersticiu byl nález difuzního lymfocytárního infiltrátu s počínající fibroprodukcí. Imunofluorescenční vyšetření odhalilo lineární depozita imunoglobulinu G (IgG) podél glomerulární bazální mebrány (obr. 2), složka C3 byla pozitivní pouze fokálně v cévách. V séru byl následně zjištěn vysoký titr anti‑GBM protilátek 18887 CU. Pacientce byl zaveden akutní hemodialyzační katétr a byla zahájena agresivní imunosupresivní léčba rychle progredující glomerulonefritidy.
Podali jsme tři pulzy methylprednisolonu (700 mg/m2) a zároveň bylo zahájeno podávání intravenózního cyklofosfamidu (6 dávek 500 mg/m2 à 3 týdny). Pacientka podstoupila sérii imunoadsorpcí (IA), celkem 18 procedur. Kortikoidní terapie byla následně převedena na perorální formu s postupným snižováním dávky. Pro anemizaci dostávala dívka během hospitalizace opakovaně transfuze erytrocytů. Pro hypertenzi jsme pacientce nasadili kombinaci betablokátoru (propranolol) a blokátoru kalciového kanálu (amlodipin) s dobrým efektem. Diuréza byla po celou dobu hospitalizace dostatečná. Pacientka byla zcela bez plicní symptomatologie, v rámci dovyšetření jsme navíc vzhledem k diagnóze doplnili výpočetní tomografii (CT) plic, která byla bez průkazu alveolární hemoragie. Po měsíčním pobytu na našem pracovišti jsme dívku propouštěli s výraznou renální lézí (glomerulární filtrace [GFR] 40 ml/min/1,73 m2), zároveň došlo k významnému poklesu koncentrace anti‑GBM protilátek k hodnotě 620 CU. Pro trvající anémii při poklesu GFR jsme zahájili podávání darbepoetinu v dávce 1 µg/kg/14 dní. Krevní tlak byl před dimisí korigován kombinovanou antihypertenzní terapií (amplodipin, propranolol, ramipril).
Aktuálně (15 měsíců od manifestace onemocnění) je dívka ve velmi dobrém klinickém stavu, prospívá, neprodělala žádnou závažnou infekci. Laboratorní hodnoty prokazují zlepšení funkce ledvin, GFR 70 ml/min/1,73 m2 (odpovídá chronickému onemocnění ledvin [CKD] 2. stupně), krevní tlak je v mezích normy na zavedené terapii, v moči přetrvává mírná proteinurie (protein‑kreatininový index 50 mg/mmol, avšak negativní albuminurie), koncentrace anti‑GBM protilátek je nízká – méně než 2,9 CU.
Komentář
Literatura
- McAdoo SP, Pusey CD. Anti‑Glomerular Basement Membrane Disease. Clin J Am Soc Nephrol 2017;12:1162–1172.
- Maliakkal JG, Hicks MJ, Michael M, et al. Renal Survival in Children with Glomerulonephritis with Crescents: A Pediatric Nephrology Research Consortium Cohort Study. J Clin Med 2020;9:2385.
- Bharati J, Jhaveri KD, Salama AD, Oni L. Anti‑Glomerular Basement Membrane Disease: Recent Updates. Adv Kidney Dis Health 2024;31:206–215.
- Gittins N, Basu A, Eyre J, et al. Cerebral vasculitis in a teenager with Goodpasture’s syndrome. Nephrol Dial Transplant 2004;19:3168–3171.
- Hellmark T, Segelmark M. Diagnosis and classification of Goodpasture’s disease (anti‑GBM). J Autoimmun 2014;48–49:108–112.
- Yang R, Hellmark T, Zhao J, et al. Levels of epitope‑specific autoantibodies correlate with renal damage in anti‑GBM disease. Nephrol Dial Transplant 2009;24:1838–1844.
- de Graeff N, Groot N, Brogan P, et al. European consensus‑based recommendations for the diagnosis and treatment of rare paediatric vasculitides – the SHARE initiative. Rheumatology 2019;58:656–671.
- Yang XF, Jia XY, Yu XJ, et al. Rituximab for the treatment of refractory anti‑glomerular basement membrane disease. Ren Fail 2022;44:1123–1129.
- Kategorie: Kazuistiky
Goodpastureova nemoc (GN), jinak také nazývaná anti‑GBM nemoc, je vzácná vaskulitida postihující malé cévy. Onemocnění je způsobeno v krvi cirkulujícími protilátkami namířenými proti bazální membráně glomerulů a plicních alveolů. V ledvinách se nemoc projeví jako rychle progredující glomerulonefritida (RPGN), v plicích vzniká alveolární krvácení, to však nemusí být přítomno u všech pacientů. Udávaná incidence GN je < 2/1 000 000 obyvatel.1 GN se typicky vyskytuje ve dvou věkových kategoriích – ve třetí dekádě a poté v šesté až sedmé dekádě života. Výskyt GN v dětském věku je extrémně vzácný, představuje pouze asi 3 % všech případů RPGN.2 Onemocnění často předchází plicní nebo renální inzult. Mezi nejčastější patří respirační infekt, kouření cigaret, litotrypse, ANCA asociovaná vaskulitida. Je popisována i léky indukovaná anti‑GBM nemoc (tab. 2).3 Pacienti udávají často v předchorobí nespecifické symptomy, jako je únava, bolesti kloubů, úbytek hmotnosti, horečky.
Manifestace GN probíhá pod obrazem RPGN v 80–90 %, plicní hemoragie různé závažnosti se rozvine u 25–60 % případů. Výjimečně se může GN projevit izolovaným plicním nálezem. Symptomatologie je variabilní a je závislá na závažnosti celkového stavu – dušnost, hemoptýza, bolesti na hrudi, hypertenze, otoky, hematurie a další. Postižen může být i centrální nervový systém, což se projeví nejčastěji vznikem křečí.4
V patogenezi nemoci hrají zásadní roli anti‑GBM protilátky třídy IgG, které se váží na α3‑řetězec kolagenu IV v glomerulární bazální membráně, který je zároveň přítomen i v alveolární bazální membráně. Tvorba protilátek může předcházet manifestaci choroby o mnoho měsíců. Následně dochází k aktivaci komplementu a k zánětlivé odpovědi neutrofilů.5 Předpokládá se, že spouštěč (infekce, environmentální faktor) iniciálně způsobí odkrytí antigenního epitopu kolagenu s následnou tvorbou anti‑GBM protilátek.6 U části pacientů pozorujeme duální pozitivitu anti‑GBM protilátek s protilátkami ANCA.
V rámci diagnostiky GN pátráme po přítomnosti anti‑GBM protilátek v séru či v bioptickém vzorku ledviny. Zvýšený titr sérových anti‑GBM protilátek zjišťujeme u 90 % pacientů. V renální biopsii typicky nacházíme RPGN a přítomnost IgG podél glomerulárních kapilár, někdy též podél distálních tubulů. Vzácně může být namísto IgG zjištěna pozitivita IgA či IgM.
Terapie dětí s GN vychází z léčebných schémat pro dospělé pacienty. Podáváme intenzivní kombinovanou imunosupresi – kortikoidy (iniciálně tři pulzy methylprednisolonu, dále prednison), cyklofosfamid, zároveň zahajujeme eliminační léčbu – plazmaferézu nebo imunoadsorpci s cílem zastavit tvorbu anti‑GBM protilátek, potlačit zánět a současně eliminovat již vytvořené protilátky a imunitní působky. Eliminační léčba je indikována do poklesu titru anti‑GBM protilátek pod detekční mez či alespoň po dobu 14 dní.7 V případě, že je podání cyklofosfamidu kontraindikováno, lze podat rituximab, monoklonální anti‑CD20 protilátku, kterou někteří autoři doporučují i jako přídatnou terapii u velmi závažných případů.8 Provedení transplantace ledviny je vhodné u jedinců v konečné fázi CKD, u kterých šest měsíců nedetekujeme anti‑GBM protilátky, jelikož jejich přítomnost zvyšuje významně riziko rekurence onemocnění. De novo anti‑GBM nemoc se může rozvinout u pacientů s X‑vázaným Alportovým syndromem. Mezi experimentální léčbu GN řadíme imlifidázu – IgG degradující enzym Streptococcus pyogenes či léky cílící na cytokiny tumor nekrotizujícího faktoru alfa (TNFα) nebo interleukin 11. Prognóza onemocnění závisí na časnosti stanovení diagnózy, většina pacientů dosáhne sérologické remise, jednoroční mortalita dospělých pacientů dosahuje < 40 %, roční přežití ledvin je 25–30 %.3 Vzhledem k minimálnímu výskytu GN v dětském věku však nemáme k dispozici pediatrická data.
Prezentujeme vzácný případ GN u batolete. Naše kazuistika dokládá, že je potřeba v diferenciální diagnostice glomerulonefritid u dětí myslet i na onemocnění, která se typicky vyskytují v dospělé populaci. Opoždění stanovení diagnózy GN u naší pacientky bylo dáno méně dramatickou manifestací nemoci i velmi raritním výskytem GN v takto časném věku.