Recidivující nefrolitiáza v ambulanci nefrologa
Souhrn
Nefrolitiáza je časté recidivující onemocnění a rizikový faktor pro vznik chronického onemocnění ledvin. Doporučení Kidney Disease: Improving Global Outcomes (KDIGO) proto považují recidivující nefrolitiázu za indikaci k nefrologickému vyšetření. Recidivám lze předcházet. Úspěšná prevence vyžaduje pečlivé laboratorní vyšetření k odhalení metabolických rizik, nastavení režimových opatření a zahájení farmakoterapie. Předmětem sdělení je diagnostický a terapeutický přístup k pacientovi s recidivující nefrolitiázou z pohledu nefrologa.
Úvod
Nefrolitiáza je časté a recidivující onemocnění, vyskytuje se asi u 10 % mužů a 5 % žen v populaci.1 Vzniká na podkladě metabolických odchylek, které přispívají k chronickému průběhu onemocnění a opakovanému vzniku konkrementů. Opakované epizody nefrolitiázy zvyšují riziko další recidivy a jsou spojeny s méně příznivou prognózou.2 Často vyžadují urologické intervence, které zhoršují kvalitu života pacienta a mohou vést k poškození renálního parenchymu.
Správně nastavená sekundárněpreventivní léčba je klíčová pro prognózu pacienta. Cílem tohoto textu je představit diagnostický a terapeutický přístup k pacientovi s recidivující nefrolitiázou z pohledu nefrologa.
Klasifikace konkrementů
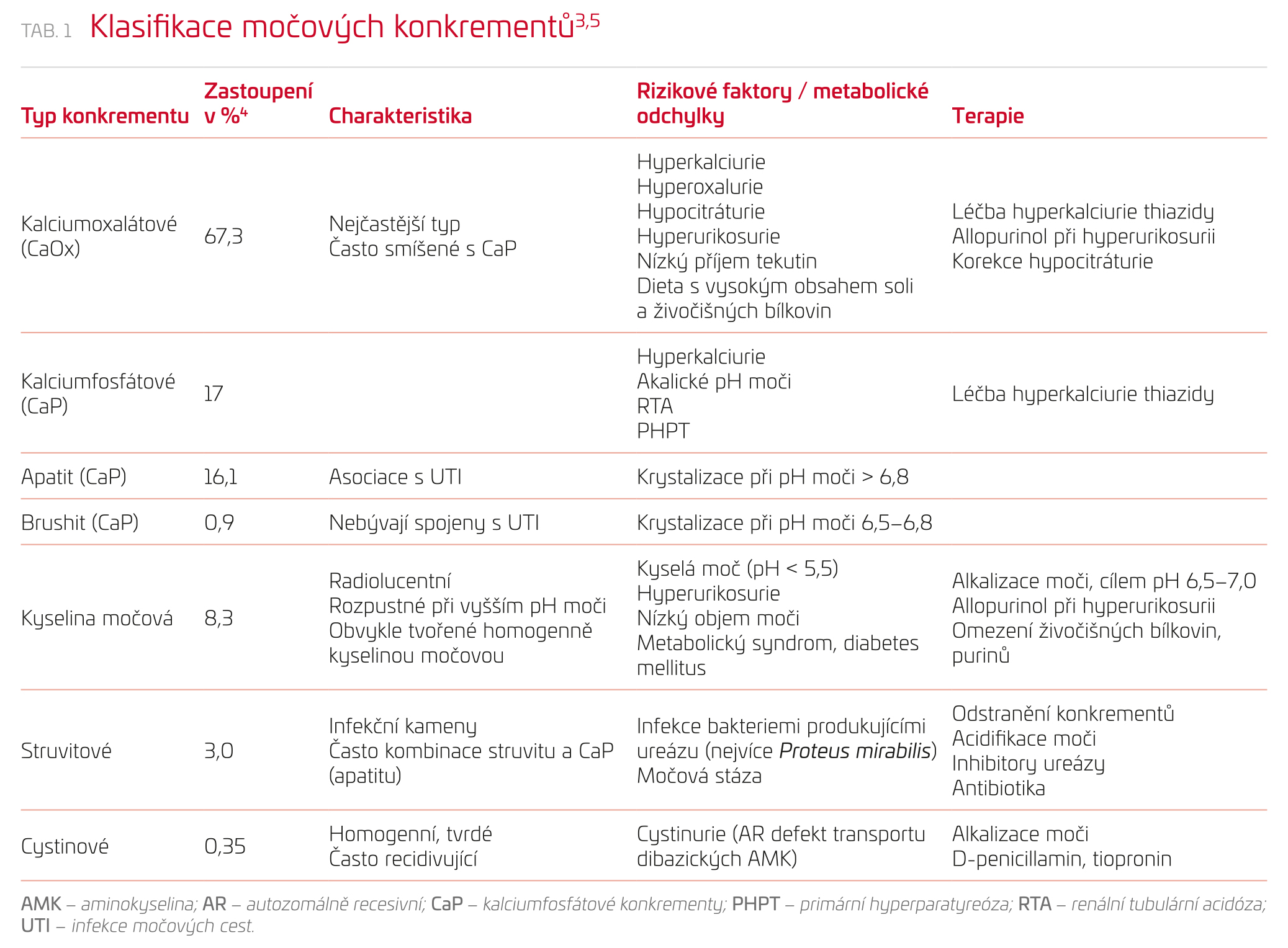
V běžné populaci se nejčastěji vyskytují kalciové konkrementy, které tvoří 70–80 % všech kamenů. Podle převažující minerální složky se dělí na kalciumoxalátové (přibližně 80 %) a kalciumfosfátové. Zastoupení struvitových kamenů je v literatuře často uváděno v rozmezí 10–15 %. Data z rozsáhlé americké kohorty čítající 43 tisíc pacientů však ukázala podíl pouze 3 %.3,4 Přehled jednotlivých typů konkrementů, rizikových faktorů a terapie uvádí tabulka 1.
Recidiva nefrolitiázy a její rizikové faktory
Recidiva nefrolitiázy je častá – vyskytuje se přibližně u 50 % pacientů během 5–10 let od první epizody. K rizikovým faktorům recidivy patří předchozí výskyt nefrolitiázy, mladší věk při první manifestaci, mužské pohlaví, pozitivní rodinná anamnéza a zvýšený index tělesné hmotnosti. Riziko recidivy je ovlivněno složením konkrementu – za zvlášť rizikové jsou považovány kameny tvořené kyselinou močovou, struvitem a brushitem.6
Souvislost mezi obezitou a výskytem nefrolitiázy byla opakovaně prokázána. U obézních pacientů se častěji tvoří kalciumoxalátové a urátové konkrementy. Novější data naznačují, že riziko recidivy nefrolitiázy roste se stoupajícím množstvím viscerálního tuku. Riziko výskytu nefrolitiázy může zvyšovat i léčba obezity (např. terapií orlistatem a bariatrickými operacemi).6,7
Diagnostický postup v ambulanci nefrologa
Hlavním krokem, který určuje terapeutický postup, je identifikace složení konkrementu. V praxi často informace o složení konkrementu chybí. Analýzu konkrementu je proto nezbytné zajistit při nejbližší příležitosti, ať už při spontánním odchodu kamene, nebo v rámci urologického výkonu. Je třeba pamatovat, že při recidivě může být složení konkrementu odlišné. Opakovaná analýza je doporučována při selhání farmakologické prevence nebo při recidivě s delším časovým odstupem od předchozí epizody.5
U pacientů s recidivující nefrolitiázou je vždy indikováno cílené metabolické vyšetření. Standardem jsou dva po sobě následující 24hodinové sběry moči, při nichž se hodnotí objem moči, pH, vylučování vápníku, oxalátu, kyseliny močové, citrátu, sodíku, draslíku a kreatininu. Doporučuje se doplnit i stanovení fosfátů, hořčíku a urey. V případech, kdy složení konkrementu není známo, může být metabolické vyšetření moči jediným vodítkem pro odhalení litogenních faktorů a nastavení cílené prevence.5
Mikroskopické vyšetření moči je užitečné především při detekci krystalů cystinu a struvitu. Naproti tomu krystaly kalciumoxalátu, kalciumfosfátu a kyseliny močové se běžně vyskytují i u zdravých jedinců, a jejich diagnostická hodnota je proto omezená.8
Součástí diagnostiky je rovněž základní laboratorní vyšetření krve, nezbytné minimum představuje stanovení koncentrace kreatininu v séru, urey, kalcemie, chloridů, draslíku, kyseliny močové a bikarbonátu.5
Recidivující nefrolitiáza spojená s hyperkalcemií může být projevem jiného základního onemocnění, nejčastěji primární hyperparatyreózy. Při přítomnosti hyperkalcemie je vždy nutné doplnit vyšetření parathormonu (PTH) a vitaminu D. Primární hyperparatyreóza je příčinou pouze 5 % případů kalciové nefrolitiázy, její přehlédnutí však může vést k nevratnému poškození renálního parenchymu.5
U pacientů s idiopatickou kalciovou nefrolitiázou a současnou hyperkalciurií, hypocitráturií a pH ranní moči > 5,8 je vhodné zvážit provedení acidifikačního testu k vyloučení nekompletní distální renální tubulární acidózy (idRTA). Ta se vyskytuje přibližně u 16 % pacientů s idiopatickou kalciovou nefrolitiázou a je spojena s častější recidivou konkrementů a nápadnější nefrokalcinózou. Diagnóza idRTA má tedy i prognostický význam.9
Terapeutický postup v ambulanci nefrologa
Režimová a dietní opatření
Způsob stravování ovlivňuje recidivu nefrolitiázy. Data svědčí ve prospěch vegetariánské diety s dostatečným přísunem mléčných výrobků.10 Nabídnutí volby mezi vegetariánstvím a recidivou nefrolitiázy by však mohlo vztah mezi lékařem a pacientem poznamenat. Vhodnější je doporučovat dietní opatření jednotlivě.
Základem je dostatečný a rovnoměrně rozložený příjem tekutin během dne. Diuréza by měla přesáhnout 2,5 litru za 24 hodin. Nevhodná je konzumace slazených kolových nápojů, která je riziková pro vznik nefrolitiázy.2,5
Nutné je omezení příjmu kuchyňské soli – denní příjem by neměl přesáhnout 4–5 g.5 Prosté doporučení „nesolit“ je vhodné rozšířit edukací o obsahu soli v některých běžných potravinách. Konkrétními příklady lze ilustrovat, jak snadno lze překročit doporučený denní limit i bez zjevně slaného jídla. Dodržování omezení příjmu sodíku lze orientačně posoudit pomocí natriurézy ve 24hodinovém sběru moči, která by neměla překročit 100 mmol.8
Ani při výskytu kalciových konkrementů by dietní příjem vápníku neměl být omezován. Nízký příjem vede ke zvýšenému vstřebávání oxalátů ve střevě a je spojen s úbytkem kostní hmoty. Doporučovaný denní příjem vápníku je 1 000–1 200 mg a měl by být zajištěn běžnou stravou. Suplementace vápníku se u pacientů s nefrolitiázou nedoporučuje, výjimkou je enterická hyperoxalurie.5,11
Omezení příjmu bílkovin představuje další preventivní opatření. Doporučený denní příjem je 0,8–1,0 g/kg tělesné hmotnosti, přičemž důraz je kladen zejména na omezení příjmu živočišných bílkovin. U pacientů s kalciumoxalátovými nebo urátovými konkrementy a současnou hyperurikosurií je vhodné omezit příjem potravin s vysokým obsahem purinů.5
Dietní oxalát nepatří mezi hlavní rizikové faktory vzniku kalciumoxalátové nefrolitiázy, což je podporováno i zjištěním, že v příjmu oxalátu není rozdíl mezi jedinci s nefrolitiázou a bez ní.1 Asi 50 % oxalátu v moči má endogenní původ, ale i tak se předpokládá jeho vyšší intestinální absorpce u jedinců s kalciumoxalátovou nefrolitiázou.2 V případě prokázané hyperoxalurie se doporučuje omezit konzumaci potravin s vysokým obsahem oxalátu, jako je špenát, rebarbora, čokoláda nebo ořechy, a vyvarovat se nadměrného příjmu vitaminu C. U pacientů bez hyperoxalurie se dietní restrikce oxalátu nedoporučuje.5
Metabolické odchylky při nefrolitiáze a jejich terapie
Metabolické odchylky jako hyperkalciurie, hypocitráturie či hyperoxalurie se podílejí na recidivě nefrolitiázy. Jejich cílená korekce představuje základ sekundární prevence. Účinnost terapie je třeba hodnotit pomocí 24hodinového sběru moči, zprvu za 8–12 týdnů po jejím zahájení, dále každých 12 měsíců.5
Hyperkalciurie
Podávání thiazidových diuretik je zavedenou metodou prevence recidivy kalciové nefrolitiázy. V běžné praxi je nejčastěji volen hydrochlorothiazid (HCT) v dávce 25 mg dvakrát denně. V roce 2023 však výsledky studie NOSTONE12 zavedený postup zpochybnily. Ve srovnání s placebem nebyl prokázán signifikantní rozdíl v četnosti recidiv ani při dávkách HCT 50 mg denně. Evropská urologická asociace (EAU) upozorňuje, že hodnoty kalciurie u pacientů ve studii nedosahovaly hranice 8 mmol/den, při které je léčba thiazidy doporučena.5 Vztah mezi kalciurií a rizikem litiázy je však spojitý a uvedená prahová hodnota je do značné míry arbitrární.
Při terapii thiazidy je nutné monitorovat kalemii – hypokalemie může vést ke zvýšené renální reabsorpci citrátu.6 Podmínkou efektu thiazidů je současná restrikce sodíku v dietě.
Hypocitráturie
Citrát inhibuje tvorbu, růst a agregaci krystalů. Při jeho podávání pacientům s kalciumoxalátovými kameny byl efekt popsán i u normocitráturie. Naproti tomu při kalciumfosfátové nefrolitiáze je role citrátu kontroverzní. Tito pacienti mívají vyšší hodnotu pH moči a další alkalizace může podpořit tvorbu konkrementů. Rozhodnutí o podání citrátu by proto mělo být individuální, nutná je pravidelná monitorace pH moči.2
To lze ilustrovat příkladem mladé pacientky z naší ambulance s distální RTA při Sjögrenově syndromu a odlitkovou kalciumfosfátovou nefrolitiázou. Nutná je korekce metabolické acidózy (která zvyšuje kalciurii a fosfaturii), ideálně citrátem draselným (sodné soli mohou zvyšovat kalciurii). Snažíme se i zvýšit citráturii. To by však při dobře korigované metabolické acidóze nemělo být na úkor vzestupu hodnoty pH moči > 7. Riziko litogeneze při nižších koncentracích citrátu v moči můžeme snížit podáním thiazidu.
Hyperurikosurie
Zvýšené vylučování kyseliny močové je pozorováno přibližně u třetiny pacientů s kalciumoxalátovou nefrolitiázou a je považováno za rizikový faktor její recidivy. Častěji se vyskytuje u starších pacientů a jedinců s metabolickým syndromem. Při hyperurikosurii je doporučováno omezit příjem purinů ve stravě, při exkreci kyseliny močové nad 4 mmol/den zahájit léčbu allopurinolem v dávce 100 mg denně, která se navyšuje při současné hyperurikemii.2,5,12,13
Hypeurikosurie je nikoliv překvapivě rizikovým faktorem vzniku konkrementů z kyseliny močové. Terapie allopurinolem se řídí stejnými zásadami jako u kalciumoxalátové litiázy. Hlavním krokem v prevenci urátové litiázy je alkalizace moči, cílové pH moči je 6,5–7,0. Doporučované dávky citrátu jsou 3–10 g/den, nejčastěji se používá citrát draselný.5,6
Hyperoxalurie, cystinurie
Hyperoxalurie, definovaná jako vylučování oxalátu močí > 0,5 mmol/den, patří k nejběžnějším laboratorním nálezům u pacientů s nefrolitiázou. Nejčastěji se jedná o sekundární (enterickou) hyperoxalurii, která je podmíněna zvýšenou střevní absorpcí oxalátu – například po bariatrických operacích nebo při malabsorpci tuků. Základem léčby enterické hyperoxalurie je perorální suplementace vápníku – váže ve střevě oxalát a brání jeho vstřebávání.5
Exkrece oxalátu nad 1 mmol/den by měla vždy vzbudit podezření na primární hyperoxalurii – vzácnou autozomálně recesivní poruchu glyoxylátového metabolismu. Typy II a III mohou vzhledem k mírnějšímu průběhu uniknout diagnóze, a proto je nezbytné na ně aktivně pomýšlet zejména u dětí a mladých dospělých s nefrolitiázou.14
Cystinurie je vzácná genetická porucha transportu dibazických aminokyselin, jež vede k tvorbě recidivujících konkrementů. Diagnostická je přítomnost hexagonálních krystalů cystinu v moči. Léčba spočívá především v důsledné hydrataci a alkalizaci moči na hodnoty pH > 7,0.6
Hypomagneziurie
Hořčík patří k inhibitorům litogeneze, je doporučen u pacientů s kalciumoxalátovou nefrolitiázou při současné enterické hyperoxalurii nebo hypomagneziurii. Rutinní podávání hořčíku u pacientů s recidivující nefrolitiázou doporučeno není.5
Infekční nefrolitiáza
Infekční kameny jsou nejčastěji tvořeny směsí struvitu a kalciumfosfátu (apatitu), vznikají působením mikroorganismů štěpících ureu (Proteus, Klebsiella, Pseudomonas, Staphylococcus, některé kmeny Escherichia coli), které vytvářejí alkalické prostředí potřebné k precipitaci struvitu. Opakovaný nález těchto bakterií v moči by měl vést k zobrazovacímu vyšetření k vyloučení litiázy.3,15
Terapie infekční nefrolitiázy je svízelná. Infekční kameny často recidivují, mají tendenci k rychlému růstu a také jsou oproti jiným formám nefrolitiázy spojeny s vyšším rizikem terminálního selhání ledvin (ESRD). V léčbě je zásadní odstranění všech konkrementů, samotná antibiotická terapie nemůže vést k trvalé eradikaci infekce. Snížit riziko recidivy pomůže korekce metabolických odchylek, které se vyskytují i u čistě struvitové litiázy.5,16
Infekční kameny často vytvářejí odlitkovou litiázu, její kompletní odstranění vyžaduje opakované urologické výkony spojené s rizikem závažných komplikací. I parciální odstranění odlitkové nefrolitiázy však může zlepšit renální prognózu pacienta.17 Konzervativní postup při odlitkové nefrolitiáze je spojen s progresivní ztrátou renálních funkcí přibližně u 27 % pacientů.18 Management pacientů, kteří nejsou kandidáty urologické léčby, nemá jasná doporučení.
Chronické onemocnění ledvin při nefrolitiáze
Nefrolitiáza je rizikovým faktorem vzniku ESRD, přestože je jako jeho primární příčina vzácná. Riziko je vyšší u žen, obézních jedinců, pacientů s recidivujícími močovými infekcemi a struvitovou nefrolitiázou. U pacientů s recidivující nefrolitiázou je popisováno více než dvakrát vyšší riziko vzniku ESRD oproti běžné populaci.19 Paradoxně s poklesem eGFR můžeme pozorovat snížení četnosti recidiv nefrolitiázy. Tento jev je dáván do souvislosti s poklesem vylučování vápníku do moči.20
Závěr
Přestože je nefrolitiáza považována za rizikový faktor vzniku chronického onemocnění ledvin (CKD), v klinické praxi je její význam pro renální prognózu pacienta často přehlížen. Zatímco pacienti s diabetes mellitus jsou do nefrologických ambulancí referováni relativně systematicky, pacienti s recidivující nefrolitiázou se do péče nefrologa nezřídka dostávají až po opakovaných urologických intervencích – a často již s pokročilou renální dysfunkcí. Doporučení KDIGO považuje rozsáhlou recidivující nefrolitiázu za indikaci k nefrologickému vyšetření.
Pokud nelze zajistit sekundární prevenci v rámci urologické péče, je vhodné zvážit spolupráci s nefrologem, který provede komplexní vyšetření a zajistí dlouhodobé sledování. Cílem nefrologické péče není jen prevence recidivy nefrolitiázy, ale především protekce renálních funkcí a snížení rizika komplikací CKD, zejména kardiovaskulárních.
Literatura
- Taylor EN, Curhan GC. Oxalate intake and the risk for nephrolithiasis. J Am Soc Nephrol 2007;18:2198–2204.
- Zisman AL. Effectiveness of Treatment Modalities on Kidney Stone Recurrence. Clin J Am Soc Nephrol 2017;12:1699–1708.
- Espinosa‑Ortiz EJ, Eisner BH, Lange D, Gerlach R. Current insights into the mechanisms and management of infection stones. Nat Rev Urol 2019;16:35–53.
- Lieske JC, Rule AD, Krambeck AE, et al. Stone composition as a function of age and sex. Clin J Am Soc Nephrol 2014;9:2141–2146.
- Skolarikos A, Geraghty R, Somani B, et al. European Association of Urology Guidelines on the Diagnosis and Treatment of Urolithiasis. Eur Urol 2025:S0302‑2838(25)00181‑2.
- Shastri S, Patel J, Sambandam KK, Lederer ED. Kidney Stone Pathophysiology, Evaluation and Management: Core Curriculum 2023. Am J Kidney Dis 2023;82:617–634.
- Liang D, Liu C, Yang M. The association of visceral adiposity index with the risk of kidney stone and kidney stone recurrence. BMC Nephrol 2023;24:368.
- Pfau A, Knauf F. Update on Nephrolithiasis: Core Curriculum 2016. Am J Kidney Dis 2016;68:973–985.
- Sromicki J, Kacl G, Föhl M, Hess B. Prospective long‑term evaluation of incomplete distal renal tubular acidosis in idiopathic calcium nephrolithiasis diagnosed by low‑dose NH4CL loading – gender prevalences and impact of alkali treatment. J Nephrol 2022;35:1619–1626.
- Ferraro PM, Bargagli M, Trinchieri A, Gambaro G. Risk of Kidney Stones: Influence of Dietary Factors, Dietary Patterns, and Vegetarian‑Vegan Diets. Nutrients 2020;12:779.
- Worcester EM, Coe FL. Clinical practice. Calcium kidney stones. N Engl J Med 2010;363:954–963.
- Dhayat NA, Bonny O, Roth B, et al. Hydrochlorothiazide And Prevention Of Kidney‑Stone Recurrence. N Engl J Med 2023;388:781–791.
- Arowojolu O, Goldfarb DS. Treatment of calcium nephrolithiasis in the patient with hyperuricosuria. J Nephrol 2014;27:601–605.
- Hoppe B. An update on primary hyperoxaluria. Nat Rev Nephrol 2012;8:467–475.
- Bonkat G, Kranz J, Cai T, et al. EAU Guidelines On Urological Infections. Online. Dostupné z: https://uroweb.org/guidelines/urological‑infections. [citováno 2025‑06‑07].
- Danilovic A, Ferreira TAC, Gomes SA, et al. Metabolic assessment in pure struvite stones formers: is it necessary? J Bras Nefrol 2021;43:200–206.
- Teichman JM, Long RD, Hulbert JC. Long‑term renal fate and prognosis after staghorn calculus management. J Urol 1995;153:1403–1407.
- Alsawi M, Amer T, Mariappan M, et al. Conservative management of staghorn stones. Ann R Coll Surg Engl 2020;102:243–247.
- Dhondup T, Kittanamongkolchai W, Vaughan LE, et al. Risk of ESRD and Mortality in Kidney and Bladder Stone Formers. Am J Kidney Dis 2018;72:790–797.
- Rule AD, Krambeck AE, Lieske JC. Chronic kidney disease in kidney stone formers. Clin J Am Soc Nephrol 2011;6:2069–2075.
- Kategorie: Názor hosta
- Klíčová slova: dieta; chronické onemocnění ledvin; močové kameny; nefrolitiáza; rekurence