Akutní selhání ledvin při cholemické nefróze
Kazuistika
Sedmašedesátiletý pacient dosud bez významné interní anamnézy byl přijat na JIP Kliniky gastroenterologie a hepatologie Všeobecné fakultní nemocnice v Praze (VFN) překladem po krátké hospitalizaci na spádovém interním oddělení, kam byl přijat pro bezbolestný ikterus s třesavkami.
V předchorobí pacient udával užívání alkoholu po dobu dvou měsíců v podobě jednoho piva denně, v posledním měsíci před hospitalizací však požívání alkoholu striktně odmítá. Zhruba měsíc před přijetím užíval kotvičník zemní (k posílení sexuální kondice); po 14 dnech s užíváním přestal pro nevolnost a „bolest jater“. Žlutavého zabarvení kůže a sklér si všiml až po 14 dnech od konce užívání kotvičníku a rozhodl se vyhledat lékařské ošetření. Uvedl požití většího množství paracetamolu, užívání jiných léků nebo drog negoval.
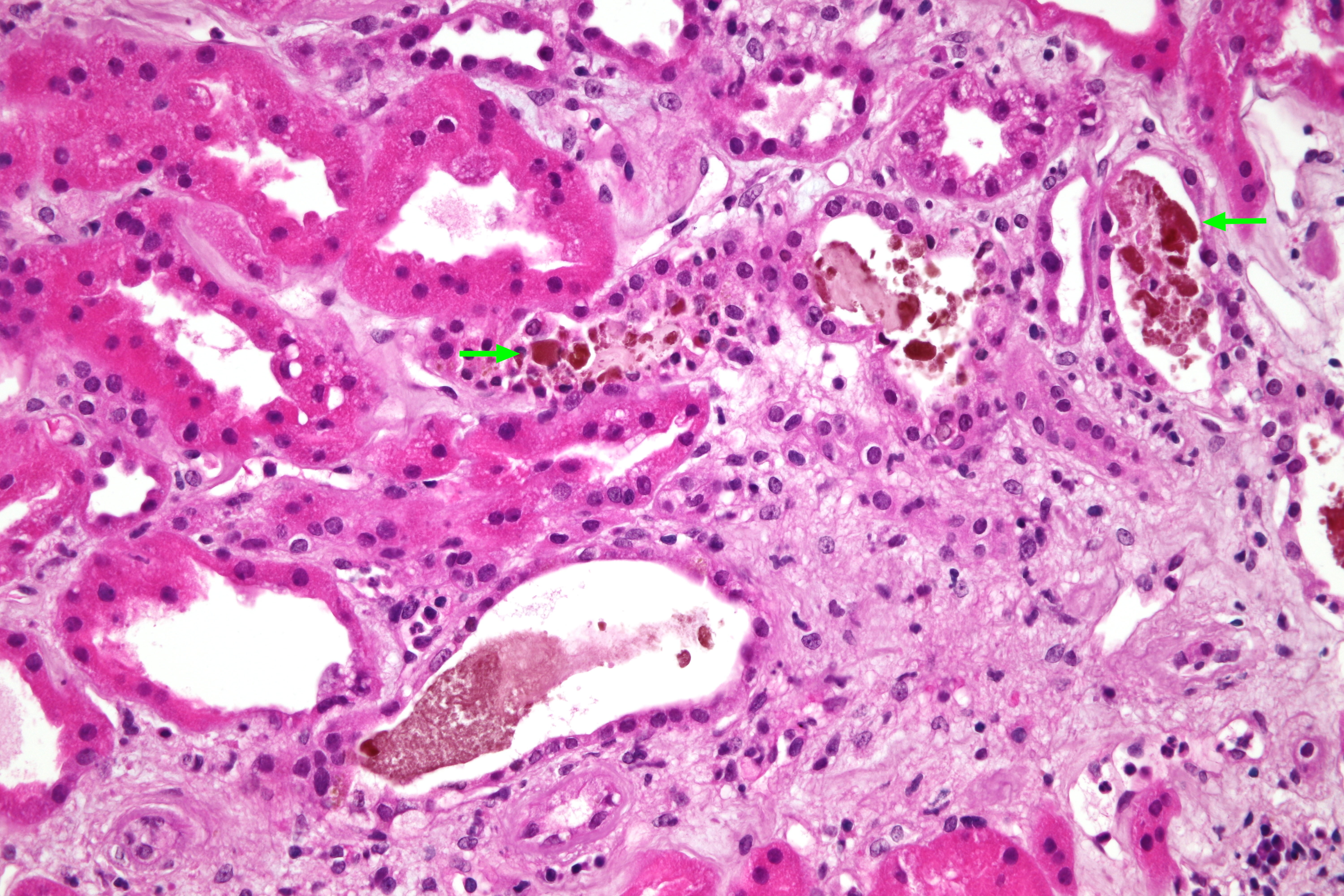
OBR. 1 Bioptický nález, barvení hematoxylinem a eosinem – morfologie akutní tubulární nekrózy, žlučové válce v tubulech označené šipkami.
Při příjmu u pacienta klinicky dominoval sytě ikterický kolorit, při vstupním laboratorním vyšetření byly hodnoty celkového bilirubinu 647 µmol/l a přímého bilirubinu 503 µmol/l, lehce zvýšená aktivita enzymu alaninaminotransferázy – 0,81 µkat/l – a aspartátaminotransferázy – 0,80 µkat/l – spolu se zvýšenou hodnotou gamaglutamyltransferázy – 3,20 µkat/l. Dále byla přítomna normocytární normochromní anémie s koncentrací hemoglobinu 99 g/l a zejména leukocytóza 26,41 × 109/l s posunem doleva, doprovázená elevací hodnot C‑reaktivního proteinu (CRP) na 189 mg/l a prokalcitoninu na 24,6 µg/l. Vstupně byly také přítomny známky oligurického akutního renálního selhání se sérovou koncentrací kreatininu 620 µmol/l (poslední známá sérová koncentrace kreatininu před rokem byla v normě) a s hodnotou urey 32 mmol/l, bez závažnější poruchy acidobazické rovnováhy a mineralogramu. Byla doplněna sonografie břicha s nálezem dilatace choledochu i intrahepatálních žlučovodů obou laloků, cholecystolitiázy v drobném (vyprázdněném či afunkčním) žlučníku a s normálním nálezem na ledvinách. Empiricky byla zahájena antibiotická terapie cefoperazonem a bylo přistoupeno k endoskopické retrográdní cholangiopankreatografii, při které byla provedena endoskopická papilotomie s extrakcí tmavého konkrementu cca 6 mm velkého. Po výkonu byl ihned viditelný odtok zkalené žluči do střeva. Laboratorně po výkonu následoval výrazný pokles hyperbilirubinemie s normalizací hodnot aminotransferáz a pokles zánětlivých parametrů. I přes intravenózní podávání kličkového diuretika progredovala u pacienta pozitivní tekutinová bilance a laboratorně narůstaly hodnoty dusíkatých katabolitů. Z těchto důvodů byl pacient následně přeložen na Kliniku nefrologie VFN.
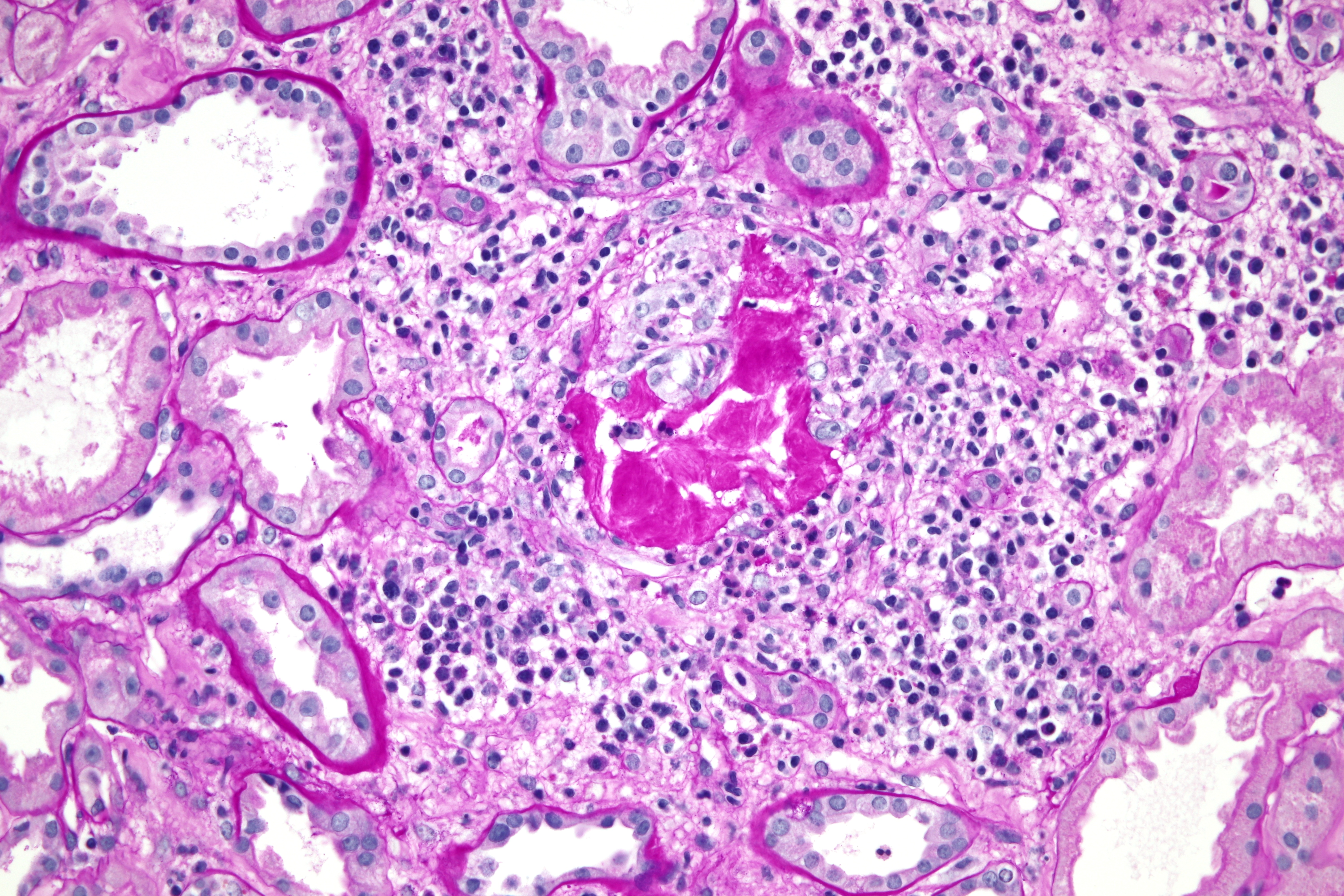
OBR. 2 Bioptický nález, barvení Periodic Acid Schiff – zánětlivá celulizace intersticia s destrukcí tubulu a Tammovým–Horsfallovým proteinem v intersticiu.
Zde byl doplněn základní imunologický screening s negativním nálezem, vyjma hodnoty C3 složky komplementu lehce snížené na 0,87 g/l. Následně jsme proto provedli renální biopsii, v níž dominovala morfologie akutní tubulární nekrózy (ATN) s četnými žlučovými válci v tubulech a projevy intrarenální obstrukce s akumulací Tammova–Horsfallova proteinu v intersticiu (obr. 1 a 2). Bioptický nález byl tedy uzavřen jako obraz cholemické nefrózy. Třetí den po renální biopsii vzhledem k dalšímu nárůstu hodnot dusíkatých katabolitů a při známkách hyperhydratace byla zahájena intermitentní hemodialýza. Celkem jsme provedli pouze dvě procedury, jelikož záhy došlo u pacienta k obnově renálních funkcí a k rozvoji mírné polyurické fáze renálního selhání. Desátý den od biopsie byl pacient v dobrém klinickém stavu propuštěn. Při poslední ambulantní kontrole dva měsíce od propuštění přetrvává elevace hodnot kreatininu 110 µmol/l, bilirubin i jaterní enzymy jsou již v normě.
Komentář
- MUDr. Hana Šafránková , Ph.D., Klinika nefrologie VFN a 1. LF UK
Literatura
- Krones E, Pollheimer MJ, Rosenkranz AR, Fickert P. Cholemic nephropathy – Historical notes and novel perspectives. Biochim Biophys Acta Mol Basis Dis 2018;1864(4 Pt B):1356–1366.
- El Chediak A, Janom K, Koubar SH. Bile cast nephropathy: when the kidneys turn yellow. Ren Replace Ther 2020;6:1–7.
- van Slambrouck CM, Salem F, Meehan SM, Chang A. Bile cast nephropathy is a common pathologic finding for kidney injury associated with severe liver dysfunction. Kidney Int 2013;84:192–197.
- Chan S, Spraggon ES, Francis L, Wolley MJ. Bile Cast Nephropathy in a Patient With Obstructive Jaundice. Kidney Int Rep 2018;4:338–340.
- Bräsen JH, Mederacke YS, Schmitz J, et al. Cholemic Nephropathy Causes Acute Kidney Injury and Is Accompanied by Loss of Aquaporin 2 in Collecting Ducts. Hepatology 2019;69:2107–2119.
- LeBlanc RM, Navar LG, Botros FT. Bilirubin exerts renoprotective effects in angiotensin II‑hypertension. Am J Med Sci 2010;340:144–146.
- Romano TG, Vieira Junior JM. Do Biliary Salts Have Role on Acute Kidney Injury Development? J Clin Med Res 2015;7:667–671.
- Somagutta MR, Jain MS, Pormento MKL, et al. Bile Cast Nephropathy: A Comprehensive Review. Cureus 2022;14(3):e23606.
- Flores A, Nustas R, Nguyen HL, Rahimi RS. Severe cholestasis and bile acid nephropathy from anabolic steroids successfully treated with plasmapheresis. ACG Case Rep J 2016;3:133–135.
- Sens F, Bacchetta J, Rabeyrin M, Juillard L. Efficacy of extracorporeal albumin dialysis for acute kidney injury due to cholestatic jaundice nephrotoxicity. BMJ Case Rep 2016;2016:bcr2015213257.
- Patel J, Walayat S, Kalva N, et al. Bile cast nephropathy: a case report and review of the literature. World J Gastroenterol 2016;22:6328–6334.
- Kategorie: Kazuistiky
- Klíčová slova: akutní renální selhání; akutní tubulární nekróza; hyperbilirubinemie; cholestáza; ikterus
Cholemická nefróza (cholemic nephropathy, CN, někdy také bile cast nephropathy, BCN) je akutní renální léze vznikající na podkladě jaterního onemocnění (cholestatické léze nebo pokročilé formy jaterního onemocnění se žloutenkou). Tento typ poškození ledvin je jistě podceňovanou příčinou akutní renální insuficience. CN je kombinací poškození funkce ledvin společně s charakteristickým histomorfologickým nálezem v ledvinách – jedná se o tvorbu intratubulárních válců a poškození epitelu tubulů převážně v oblasti distálního nefronu. Diagnostika této jednotky musí být podpořena nálezem v renální biopsii, což může být problematické hlavně pro častou přítomnost koagulační poruchy u pacientů s jaterní lézí.1
Patofyziologie vzniku poškození není zcela známá a je jistě multifaktoriální. Předpokládá se vliv vysoké koncentrace bilirubinu na funkci tubulů. Nadbytek bilirubinu poškozuje tubulární epitelie a vede k tvorbě pigmentových válců. Následně přes tubulární hypertrofii a hyperplazii dochází časem k ireverzibilnímu poškození tubulů, fibróze, a nakonec k tubulární atrofii.2 Nižší rozpustnost žlučových kyselin společně s nízkým pH v distálním nefronu přispívá také k tvorbě válců. Čím déle je organismus vystaven vysokým koncentracím bilirubinu, tím větší je tvorba žlučových válců, a tím větší je i poškození tubulů. I v případě, že dojde k relativně rychlému odstranění příčiny hyperbilirubinemie, obnova renálních funkcí může být významně opožděna.3 Podobná situace nastala i u našeho pacienta. Dalším následkem hyperbilirubinemie je pokles tlaku v ledvině ovlivněním renin‑angiotenzinového systému,4 histologicky se někdy popisuje i snížená exprese akvaporinových kanálků ve sběrných tubulech.5 Ovšem efekt bilirubinu zřejmě není jen negativní, jsou popsány i renoprotektivní účinky bilirubinu – protizánětlivý, protiapoptotický, antioxidační.1,6 Tyto účinky jsou ale při masivní hyperbilirubinemii spíše potlačeny.
Větší část žlučových kyselin je za normálních okolností reabsorbována v ileu a portálním oběhem navracena zpět do jater, do cirkulace prochází asi 10–50 %, které se následně dostávají do ledvin a v proximálním tubulu jsou reabsorbovány zpět do oběhu. Při překročení kapacity této reabsorpce výrazným zvýšením nabídky dochází k tvorbě válců a k přímému poškození tubulů.7 Žlučové kyseliny také přímo ovlivňují tvorbu vazoaktivních látek, které vedou k renální vazokonstrikci a snížení glomerulární filtrace.2
Možné příčiny cholestázy, u kterých byla popsána cholemická nefropatie, jsou popsány v článku autorů Somagutta a spol.8 Jedná se o extrahepatální příčiny obstrukce – nádorové etiologie, kameny, intrahepatální příčiny – hepatitidy virové, autoimunitní, alkoholické postižení jater, toxické poškození polékové atd. U našeho nemocného se nabízejí dvě příčiny; jednak přítomnost konkrementu v choledochu a jednak možný hepatotoxický vliv užívaného kotvičníku.
K diagnostice CN je třeba renální biopsie – v případě našeho pacienta již nažloutlé zabarvení bioptického vzorku naznačovalo diagnózu. V bioptickém nálezu bývá také podíl akutní tubulární nekrózy. Často přítomná koagulopatie však provedení biopsie komplikuje. Možné je zvážit i transjugulární přístup, kdy by bylo možné provést biopsii jater i ledvin zároveň. Bohužel diagnóza CN je někdy stanovena i post mortem.
Léčba cholemické nefrózy je primárně zaměřena na léčbu příčiny hyperbilirubinemie, vyřešení obstrukce žlučových cest. Náhrada funkce ledvin je někdy nutná, většinou jen přechodně, obnova renálních funkcí je pravděpodobná, ale není zaručena. U pacientů s cholestázou indukovanou anaboliky byla úspěšně použita plazmaferéza.9 Byla popsána i kazuistika pacienta s akutní cholestázou a renálním selháním způsobenými mutací v genu TCF2 (transcription factor 2), u kterého byla použita přechodně „albuminová dialýza“ (extracorporeal albumin dialysis, ECAD) jako překlenovací metoda k transplantaci jater a ledvin.10 Zdá se, že efekt použití kortikosteroidů, kyseliny ursodeoxycholové nebo laktulózy je minimální.11 U našeho pacienta bylo nutné provedení dvou dialýz a k normalizaci renálních parametrů došlo do dvou měsíců.
Závěrem lze říci, že diagnóza cholemické nefrózy je i v dnešní době spíše raritní záležitostí, avšak z klinické praxe vidíme, že podíl a vliv hepatálního poškození na rozvoj akutní renální insuficience či zhoršení již známé renální insuficience jsou jistě výrazně vyšší, a proto je třeba na ně myslet.