Kostní a minerálová nemoc asociovaná s chronickým onemocněním ledvin u malých dětí
SOUHRN
Kostní a minerálová nemoc asociovaná s chronickým onemocněním ledvin (CKD‑MBD) představuje jednu z nejzávažnějších komplikací chronického onemocnění ledvin (CKD). Časná diagnostika a adekvátní terapie CKD‑MBD jsou obzvláště důležité v dětském věku, kdy dochází k vývoji skeletu a cévního systému. Naprosto zásadní v terapii CKD‑MBD jsou dietní doporučení, v současnosti máme navíc k dispozici řadu přípravků, kterými můžeme vývoj CKD‑MBD ovlivnit. V případě perzistentní nekontrolovatelné hyperparatyreózy je ke zvážení zahájení dialýzy, výjimečně je nutno přistoupit k paratyreoidektomii. V tomto přehledovém článku jsou shrnuta aktuální doporučení pro přístup k malým dětem s CKD‑MBD.
Úvod
Kostní metabolismus představuje kontinuální proces novotvorby a mineralizace kosti osteoblasty a současně probíhající resorpce a remodelace kosti osteoklasty. Remodelace kosti je závislá nejen na interakci kostních buněk, ale i minerálů, některých hormonů a dalších faktorů, jako je svalová aktivita a hmotnostní zatížení kostí. Dětství a adolescence jsou zásadním obdobím pro formování zdravého skeletu i cévního systému. Právě v dětském věku může porucha regulace kostního metabolismu vést k růstovému selhávání, kostním deformitám a v neposlední řadě k postižení kardiovaskulárního systému. Ledviny hrají důležitou roli v regulaci minerálové a kostní homeostázy. Mají zásadní vliv na metabolismus vápníku i fosforu, fibroblastového růstového faktoru 23 (FGF23) a na tvorbu aktivovaného vitaminu D. Také účinek parathormonu (PTH) se projeví působením na ledviny ovlivněním vstřebávání minerálů. Recentně byla publikována doporučení Evropské společnosti pro dětskou nefrologii pro diagnostiku a léčbu kostní a minerálové nemoci asociované s chronickým onemocněním ledvin, z anglického chronic kidney disease‑metabolic bone disease (CKD‑MBD) u malých dětí.1 Předmětem tohoto sdělení je shrnout současný přístup k diagnostice a léčbě CKD‑MBD právě u dětí nejnižší věkové kategorie.
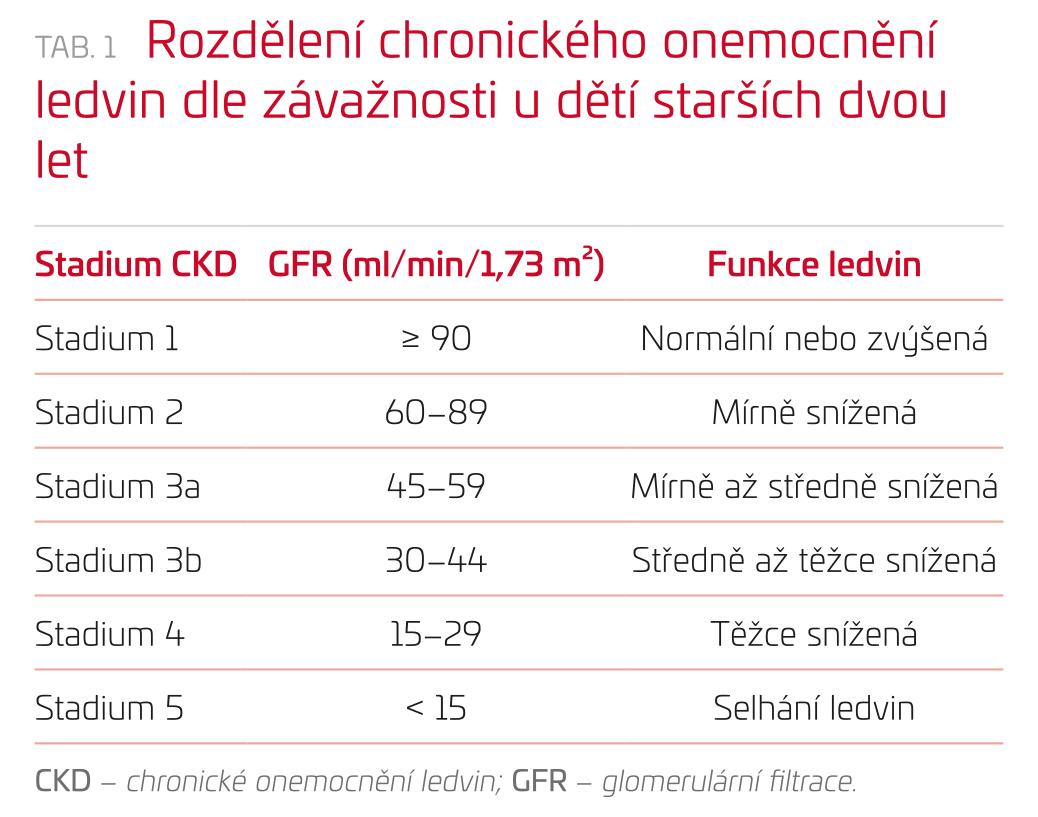
Chronické onemocnění ledvin (CKD) je v dětském věku definováno jako ireverzibilní renální strukturální nebo funkční postižení trva-jící po dobu alespoň tří měsíců, které je spojeno s progresivní ztrátou funkce ledvin. Dle závažnosti jej lze rozdělit do pěti stadií (tab. 1).2 Hodnotí se také albuminurie. Děti mladší dvou let mají nižší glomerulární filtraci, a proto pro ně používáme jiné normální hodnoty.
Patologický vliv CKD na metabolismus elektrolytů, vitaminu D, hormonů a stav kostí shrnujeme pod pojmem CKD‑MBD. Definujeme jej jako přítomnost alespoň jedné z následujících patologií:3
- abnormality metabolismu kalcia, fosforu, PTH, FGF23 a vitaminu D;
- abnormality kostního obratu, mineralizace, objemového růstu či síly kosti;
- extraskeletální kalcifikace.
Renální osteodystrofie charakterizuje změny v kostní morfologii, které vznikly následkem CKD. Rozeznáváme čtyři subtypy renální osteodystrofie:4
- osteitis fibrosa cystica – typicky následek elevace hodnot PTH, vysoký kostní obrat, zvýšení počtu i aktivity osteoblastů i osteoklastů, progrese fibrózy dřeně;
- adynamická kostní nemoc – vzniká obvykle následkem přílišné suprese PTH, nízký kostní obrat, snížení počtu i aktivity osteoblastů a osteoklastů;
- osteomalacie – snížená mineralizace kosti, může být spojena s vysokým i nízkým kostním obratem, zvýšený objem osteoidu;
- smíšená uremická osteodystrofie – kombinace osteitis fibrosa cystica a osteomalacie, vysoký kostní obrat a abnormální mineralizace.
Patogeneze CKD‑MBD
Prvotní spouštěcí mechanismus není vždy zcela jasný, ale u části pacientů dochází již v časných stadiích CKD k elevaci hodnot fosfaturického hormonu FGF23. V této době je koncentrace fosforu i PTH v séru ještě obvykle v normě. S další progresí CKD elevace koncentrace FGF23 způsobuje zvýšenou exkreci fosforu a sníženou syntézu aktivního 1,25‑dihydroxyvitaminu D, což vede ke sníženému vstřebávání kalcia a fosforu. V patogenezi se dále uplatňuje další fosfaturický hormon – PTH, který současně stimuluje syntézu 1,25‑dihydroxyvitaminu D, jenž zvyšuje enterální absorpci kalcia i fosforu. Vlivem působení FGF23 jsou ale koncentrace 1,25‑dihydroxyvitaminu D snížené, což spolu se sníženou koncentrací kalcia v séru vede ke zvýšení hodnot PTH. Kostní tkáň se stává rezistentní k působení 1,25‑dihydroxyvitaminu D i působením uremických toxinů.5 Následkem hyperparatyreózy dochází ke zvýšení kostního obratu a k resorpci a demineralizaci kosti. Současně pozorujeme vzhledem ke zvýšeným koncentracím kalcia a fosforu v séru jejich ukládání do stěny cév a do měkkých tkání.6
Vyšetření dítěte s podezřením na CKD‑MBD
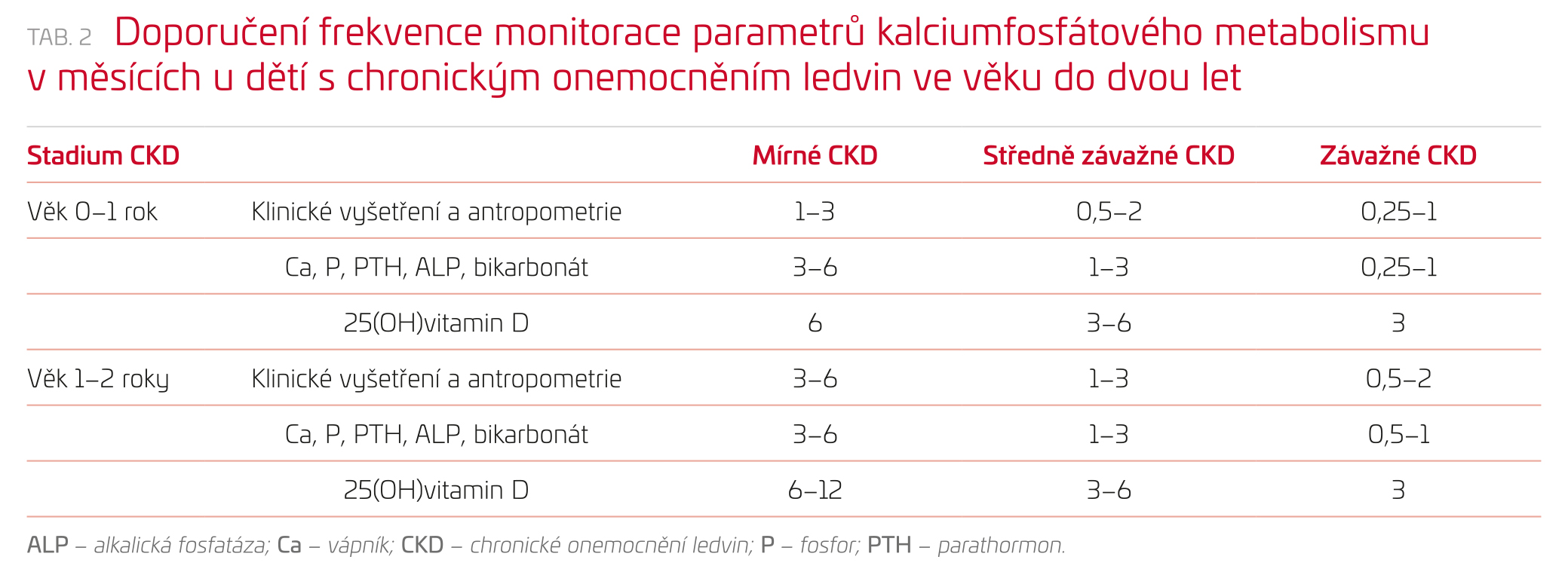
Po odebrání anamnézy se ve fyzikálním vyšetření zaměřujeme na příznaky kostní nemoci. Zajímá nás délka/výška, hmotnost a obvod hlavy dítěte, hodnoty v čase zaznamenáváme do růstových grafů. Posuzujeme psychomotorický vývoj dítěte. Pátráme po případných kostních deformitách či po známkách rachitidy, jako jsou rozšířená zápěstí, zesílení přechodu kostěné a chrupavčité části žeber (rachitický růženec), cirkulární rýha deformující distální část hrudníku (Harrisonova rýha), deformity dlouhých kostí v době, kdy mají končetiny již funkční zapojení. Současně jsou nutné pravidelné kontroly biochemických ukazatelů CKD‑MBD. U dětí s CKD 2. a vyššího stupně odebíráme krev k posouzení koncentrací kalcia v séru včetně ionizované formy, fosforu, alkalické fosfatázy, 25(OH)vitaminu D, PTH a bikarbonátu. K hodnocení bychom měli používat věkově vázané normy, protože např. potřeba kalcia je v určitých obdobích vyšší (v prvním roce života a v pubertě). Intenzivní dialýza může vést k chronické hypokalcemii, hypofosfatemii s následkem nedostatečné mineralizace kostí, může tak dojít ke vzniku rachitidy.7 Frekvenci kontroly parametrů kalciumfosfátového metabolismu u malých dětí s CKD ukazuje tabulka 2.
Vzhledem k postupné hormonální regulaci by se koncentrace PTH neměly hodnotit před jedním měsícem života ani u dětí s pokročilým CKD a také ne později než ve věku tří měsíců u jedinců s mírnější formou CKD. Naopak koncentrace 25(OH)vitaminu D u dětí s CKD bychom měli zjišťovat časněji, ideálně v prvních dvou týdnech života. Následně není obvykle zapotřebí koncentrace 25(OH)vitaminu D monitorovat častěji než jednou za tři měsíce. Výjimkou jsou pouze nedonošení novorozenci.8 Koncentraci bikarbonátu bychom měli udržovat v normě, u starších dětí na hodnotě ≥ 22 mmol/l. Nedostatečně korigovaná metabolická acidóza je známým rizikovým faktorem progrese CKD.9
Zobrazovací metody u dětí s CKD
Rentgenové snímky kostí by se u dětí s podezřením na CKD‑MBD neměly provádět rutinně. Přínosné mohou být u malých dětí a u jedinců s nedostatečně kompenzovanou kostní nemocí. Standardně také neprovádíme magnetickou rezonanci, sonografii kostí či duální rentgenovou absorpciometrii.1
Léčba CKD‑MBD
Cílem terapie je udržení koncentrací kalcia, fosforu a alkalické fosfatázy v séru v normálním rozmezí pro daný věk dítěte. V současné době nemáme jasná data pro určení optimálních koncentrací PTH u dětí s CKD. Většina expertů doporučuje cílovou hodnotu pro děti s CKD ve stadiu 1–3 v normálním rozmezí, ve stadiu 4 mírně nad normou a ve stadiu 5 v rozmezí dvojnásobku až trojnásobku horní normy pro PTH.10 Součástí týmu pečujícího o děti s CKD má být nutriční specialistka se zkušeností s danou problematikou. Příjem kalcia ze stravy a z medikace by neměl přesahovat dvojnásobek denního doporučeného příjmu (tab. 3). Výjimkou mohou být např. pacienti v období růstového spurtu či malé děti léčené intenzivní hemodialýzou, kdy mohou být nároky na příjem kalcia vyšší. Pokud není příjem kalcia stravou dostatečný, lze jej u dětí s hyperparatyreózou suplementovat, u dialyzovaných pacientů lze použít roztok s vyšší koncentrací kalcia. V případě rozvoje hyperfosfatemie či sekundární hyperparatyreózy by příjem fosforu měl být na dolní hranici denního doporučeného příjmu. Je potřeba mít na paměti, že normální hodnoty fosforu u malých dětí jsou vyšší než u dětí starších. Naopak u dětí s hypofosfatemií je nutná substituce fosforu. Kojení je preferovanou metodou krmení malých dětí. Pokud si matka nepřeje kojit nebo kojit nemůže, je vhodné děti krmit umělým mlékem s vyšším zastoupením syrovátky v poměru ke kaseinu.

Máme k dispozici i umělá mléka pro děti s pokročilým CKD s nižším obsahem kalcia a fosforu.11 Základem restrikce příjmu fosforu je omezení konzumace zpracovaných potravin a živočišných bílkovin. Omezení příjmu fosforu by ale nemělo vést k nízké konzumaci bílkovin a kalcia. Při nedostatečné kontrole fosfatemie stravou podáváme dětem vazače fosforu (tab. 4); na prvním místě kalciové vazače fosforu, při rozvoji hyperkalcemie přistupujeme k léčbě sevelamer karbonátem. Účinnost a bezpečnost podání sevalamer karbonátu u dětí mladších šesti let však nebyly dostatečně studovány. Všichni novorozenci a kojenci by v prvním roce života měli dostávat nativní vitamin D, jehož koncentrace by se měla u dětí s CKD pohybovat v rozmezí 75–120 nmol/l. Aktivní vitamin D podáváme v co nejnižší dávce s cílem normalizovat hodnoty kalcia a cílové koncentrace PTH. Vitamin D (nativní, aktivní) by dítě mělo užívat ústy, nikoliv sondou či podáním do gastrostomie. Perzistentní nekontrolovaná hyperparatyreóza je důvodem ke zvážení zahájení/optimalizace dialýzy. U pacientů s nekontrolovanou přetrvávající závažnou hyperparatyreózou, kteří jsou adekvátně konzervativně léčeni, můžeme přistoupit k léčbě cinakalcetem za předpokladu, že sérové koncentrace kalcia jsou v pásmu vyšší normy či v pásmu hyperkalcemie. Rizikem léčby cinakalcetem je rozvoj symptomatické hypokalcemie.12 Podávání cinakalcetu je indikováno u dětí starších tří let, ve výjimečných případech se může použít i u dialyzovaných dětí v časnějším věku za důsledného monitorování parametrů kalciumfosfátového metabolismu.13 Při úplném selhání konzervativní léčby je namístě provedení paratyreoidektomie.1
Literatura
- Bacchetta J, Schmitt CP, Bakkaloglu SA, et al. Diagnosis and management of mineral and bone disorders in infants with CKD: clinical practice points from the ESPN CKD‑MBD and Dialysis working groups and the Pediatric Renal Nutrition Taskforce. Pediatr Nephrol 2023;38:3163–3381.
- Kidney Disease: Improving Global Outcomes CKD Work Group. KDIGO 2024 Clinical Practice Guideline for the Evaluation and Management of Chronic Kidney Disease. Kidney Int 2024;105(4S):S117–S314.
- Kidney Disease: Improving Global Outcomes CKD‑MBD Update Work Group. KDIGO 2017 Clinical Practice Guideline Update for the Diagnosis, Evaluation, Prevention, and Treatment of Chronic Kidney Disease‑Mineral and Bone Disorder (CKD‑MBD). Kidney Int Suppl (2011) 2017;7:1–59.
- Wesseling‑Perry K, Salusky IB. Chronic kidney disease: mineral and bone disorder in children. Semin Nephrol 2013;33:169–179.
- Ayoob RM, Mahan JD. Pediatric CKD‑MBD: existing and emerging treatment approaches. Pediatr Nephrol 2022;37:2599–2614.
- Hanudel MR, Salusky IB. Treatment of Pediatric Chronic Kidney Disease‑Mineral and Bone Disorder. Curr Osteoporos Rep 2017;15: 198–206.
- Ketteler M, Block GA, Evenepoel P, et al. Executive summary of the 2017 KDIGO Chronic Kidney Disease‑Mineral and Bone Disorder (CKD‑MBD) Guideline Update: what’s changed and why it matters. Kidney Int 2017;92:26–36.
- Burris HH, Van Marter LJ, McElrath TF, et al. Vitamin D status among preterm and full‑term infants at birth. Pediatr Res 2014;75:75–80.
- Harambat J, Kunzmann K, Azukaitis K, et al. Metabolic acidosis is common and associates with disease progression in children with chronic kidney disease. Kidney Int 2017;92:1507–1514.
- Bakkaloglu SA, Bacchetta J, Lalayiannis AD, et al. Bone evaluation in paediatric chronic kidney disease: clinical practice points from the European Society for Paediatric Nephrology CKD‑MBD and Dialysis working groups and CKD‑MBD working group of the ERA‑EDTA. Nephrol Dial Transplant 2021;36:413–425.
- Shaw V, Anderson C, Desloovere A, et al. Nutritional management of the infant with chronic kidney disease stages 2‑5 and on dialysis. Pediatr Nephrol 2023;38:87–103.
- Bacchetta J, Schmitt CP, Ariceta G, et al. Cinacalcet use in paediatric dialysis: a position statement from the European Society for Paediatric Nephrology and the Chronic Kidney Disease‑Mineral and Bone Disorders Working Group of the ERA‑EDTA. Nephrol Dial Transplant 2020;35:47–64.
- Bernardor J, Flammier S, Zagozdzon I, et al. Safety and Efficacy of Cinacalcet in Children Aged Under 3 Years on Maintenance Dialysis. Kidney Int Rep 2024;9:2096–2109.
- Kategorie: Přehledové články
- Klíčová slova: cinakalcet; CKD minerálové a kostní onemocnění; děti; dialyzační léčba; kostní metabolismus; sekundární hyperparatyreóza; vazač fosforu