Ambulantní antibiotická léčba u pacientů s chronickým onemocněním ledvin
Pacienti s chronickým onemocněním ledvin mají vyšší riziko infekce. Infekce je druhou nejčastější příčinou úmrtí pacientů v dialyzačním programu, představuje častou komplikaci u pacientů léčených imunosupresivní léčbou po transplantaci ledvin nebo při glomerulonefritidě. Antibiotická léčba musí být dostatečně účinná. Dávky některých antibiotik se upravují podle funkce ledvin. Dávky léků vylučovaných renálně se obvykle redukují při poklesu glomerulární filtrace pod 1 ml/s/1,73 m2 o 50 % a při poklesu pod 0,5 ml/s/1,73 m2 se dávka redukuje o 50 % a interval podávání se prodlužuje. Pacientům léčeným hemodialýzou se lék podává po hemodialýze. Při antibiotické léčbě je třeba přihlédnout k další chronické medikaci a dávky ostatních léků upravit nebo jejich podávání přerušit.
Souhrn
Pacienti s chronickým onemocněním ledvin mají vyšší riziko infekce. Infekce je druhou nejčastější příčinou úmrtí pacientů v dialyzačním programu, představuje častou komplikaci u pacientů léčených imunosupresivní léčbou po transplantaci ledvin nebo při glomerulonefritidě. Antibiotická léčba musí být dostatečně účinná. Dávky některých antibiotik se upravují podle funkce ledvin. Dávky léků vylučovaných renálně se obvykle redukují při poklesu glomerulární filtrace pod 1 ml/s/1,73 m2 o 50 % a při poklesu pod 0,5 ml/s/1,73 m2 se dávka redukuje o 50 % a interval podávání se prodlužuje. Pacientům léčeným hemodialýzou se lék podává po hemodialýze. Při antibiotické léčbě je třeba přihlédnout k další chronické medikaci a dávky ostatních léků upravit nebo jejich podávání přerušit.
Chronické onemocnění ledvin (chronic kidney disease, CKD) představuje celou škálu onemocnění s různou mírou renální insuficience. Pacienti s chronickým onemocněním ledvin jsou velmi často imunokompromitovaní a mají vyšší riziko infekce. Infekční onemocnění je akutní stav, který nezřídka řeší lékař pohotovostní služby nebo praktický lékař. Antibiotická léčba musí být dobře zvolena. Dávka musí být dostatečně účinná a léčba musí probíhat po dostatečně dlouhou dobu. U pacientů se selháním ledvin je třeba dávku většiny antibiotik redukovat s ohledem na reziduální renální funkci. Některá antibiotika nelze u pacientů se selháním ledvin použít. Cílem tohoto článku je seznámit praktické lékaře a ambulantní specialisty s úskalími antibiotické léčby u pacientů trpících chronickým onemocněním ledvin.
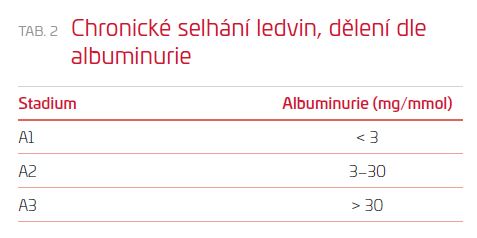
Chronické onemocnění ledvin je definováno jako onemocnění trvající minimálně tři měsíce. Dělí se podle glomerulární filtrace do pěti stadií označených jako G1–G5 a podle přítomnosti proteinurie do tří stadií – A1–A3. Dělení podle glomerulární filtrace a přítomnosti albuminurie uvádí tabulka 1 a 2. Při dávkování léčiv v naprosté většině přihlížíme ke glomerulární filtraci, proteinurie je z hlediska farmakokinetických změn méně důležitá. Pacient s chronickým selháním ledvin má glomerulární filtraci nižší než 0,25 ml/s/1,73 m2 (stadium G5) a dialyzační léčba se zahajuje podle doporučení při poklesu renální funkce pod hodnotu 0,1 ml/s/1,73 m2. Pacient s chronickým selháním ledvin je léčen dialýzou (peritoneální, hemodialýzou) nebo transplantací ledvin.1 Pacienti starší a polymorbidní mají často přínos z konzervativní léčby, kdy se dialyzační léčba nezahajuje a pacient je léčen tak, aby neměl symptomy selhání ledvin (nechutenství, syndrom neklidných nohou, svědění, metabolickou acidózu nebo příznaky anémie).2
Pacienti s chronickým onemocněním ledvin mohou být léčeni imunosupresivní terapií, kromě pacientů po transplantaci ledvin jsou to nemocní trpící glomerulonefritidou nebo jinou systémovou chorobou. Obvykle se používá kombinovaná imunosuprese kortikosteroidy s alkylačním cytostatikem (cyklofosfamid – Endoxan – nebo chlorambucil – Leukeran) s kalcineurinovými inhibitory (cyklosporin – Sandimmun Neoral, takrolimus – Prograf, Advagraf, Envarsus) nebo s mykofenolátem (Cellcept, Myfortic). V udržovacím režimu se podává azathioprin (Imuran) nebo mykofenolát s malou dávkou kortikosteroidů. Pacienti, u nichž dochází k pravidelným relapsům onemocnění nebo jsou ohroženi vyšším rizikem infekce, jsou léčeni tzv. biologickou léčbou, například rituximabem (monoklonální anti‑CD20 protilátka – Mabthera, Truxima).3
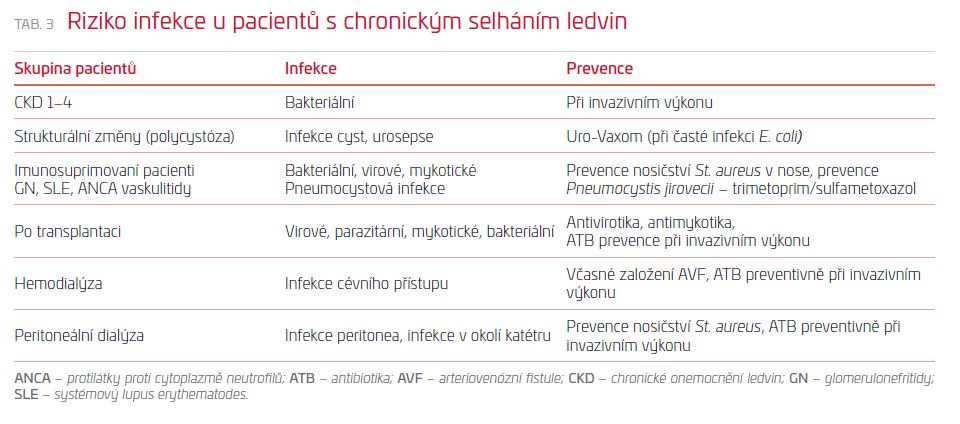
Pacienti s onemocněním ledvin a se sníženou renální funkcí mají v důsledku změn v humorální a buněčné imunitě vyšší riziko infekce. Riziko se zvyšuje u polymorbidních pacientů, diabetiků a pacientů starších 75 let. Infekce je druhou nejčastější příčinou úmrtí pacientů v dialyzačním programu. Pacienti hemodialyzovaní a peritoneálně dialyzovaní mají kromě infekcí běžných v obecné populaci infekce specifické pro dialyzované pacienty.4 Infekce cévního přístupu je častou infekční komplikací u hemodialyzovaných pacientů. Největší riziko infekce hrozí pacientům s centrálním katétrem, nejnižší riziko mají pacienti s nativní arteriovenózní píštělí.5 Peritoneálně dialyzovaní pacienti jsou ohroženi peritonitidou nebo infekcí v okolí vyústění peritoneálního katétru a infekcí podkožního tunelu. Riziko vzniku peritonitidy se zavedením důslednějších konektorových systémů snížilo. Incidence by měla být nižší než jedna peritonitida za 24 měsíců léčby. V České republice je incidence jedna peritonitida za 46 měsíců léčby.6 Většina peritonitid je vyvolána grampozitivními kmeny bakterií, které pronikají do peritoneální dutiny cestou peritoneálního katétru při nesprávně prováděné výměně dialyzačního roztoku. Méně častá je peritonitida gramnegativní, která vzniká přestupem bakterií přes stěnu střevní. Peritonitida se projevuje bolestí břicha, teplotou a zkaleným dialyzátem.7 Pacienti jsou po transplantaci ledvin, zejména v prvním roce, kdy je i imunosupresivní léčba nejagresivnější, ohroženi vysokým rizikem infekce. Kromě bakteriálních infekcí mají infekce virové (cytomegalovirus [CMV], virus Epsteina a Barrové [EBV], hepatitida typu B, C), parazitární a mykotické.8,9 Podobně jsou na tom i pacienti s imunosupresivní léčbou pro glomerulonefritidu nebo systémové onemocnění, jehož součástí je postižení ledvin (ANCA [AntiNeutrophil Cytoplasmic Antibodies, protilátky proti cytoplazmě neutrofilů] asociovaná vaskulitida, systémový lupus erythematodes, amyloidóza AL). Pacientům s polycystickou chorobou ledvin nebo s urologickým onemocněním (urolitiáza) a pacientům s diabetem hrozí vyšší riziko močové infekce, od prosté cystitidy až po akutní pyelonefritidu často komplikovanou urosepsí. Vyšší riziko močové infekce a akutní pyelonefritidy mají i těhotné ženy. Riziko infekce u pacientů s CKD je uvedeno v tabulce 3.
Lékař, který zvažuje zahájení antibiotické léčby u pacientů s chronickým onemocněním ledvin, musí vzít v úvahu několik důležitých faktorů:
- Jedná se o akutní infekci, kterou lze zvládnout podáním perorálního antibiotika, nebo je indikována parenterální antibiotická léčba za hospitalizace?
- Užívá pacient léky potlačující imunitní systém (kortikosteroidy, cyklofosfamid – Endoxan – a další léky)?
- Je pacient jinak imunitně kompromitován (diabetes mellitus, kardiální selhání)?
- Je pacient léčen hemodialýzou nebo peritoneální dialýzou? Je pacient po transplantaci ledviny?
Polymorbidní pacient, například diabetik trpící kardiovaskulárním onemocněním a pokročilou renální insuficiencí, s vysokými zánětlivými parametry s podezřením na infekci dolních cest dýchacích nebo akutní pyelonefritidu by měl být léčen parenterálně antibiotiky při hospitalizaci. Pacient po transplantaci ledvin, který je léčen imunosupresivní terapií, by měl být léčen v příslušném transplantačním centru nebo by mělo být transplantační centrum konzultováno. Obvykle je třeba snížit imunosupresivní terapii a zvýšit dávku kortikosteroidů. Pacient po snížení imunosuprese je ohrožen ztrátou funkce ledvinného štěpu.
Pacienti s různým stupněm renální insuficience při nezávažné infekci mohou být léčeni perorálním antibiotikem doma. Léčbu zahajuje lékař první pomoci nebo praktický lékař. Pacienti léčení imunosupresivní léčbou mohou mít v důsledku imunosuprese příznaky infekce méně vyjádřeny. V některých případech bývá velmi obtížené rozhodnout, zda se jedná o infekci, nebo naopak o relaps onemocnění. Teplota, vyšší hodnota C‑reaktivního proteinu může být projevem infekce nebo aktivity onemocnění. Pokles počtu bílých krvinek, především lymfocytů, může být způsoben virovou infekcí nebo imunosupresivní léčbou, naopak kortikosteroidy způsobují leukocytózu. Imunosuprimovaní pacienti s bakteriální infekcí mají být léčeni podle citlivosti antibiotikem v dávce upravené podle funkce ledvin. Kombinovaná imunosupresivní terapie se upravuje po konzultaci s ošetřujícím nefrologickým nebo revmatologickým pracovištěm. Imunosupresivní léčba se buď přeruší v případě alkylačních cytostatik, nebo se snižuje. Dávka mykofenolátu se snižuje na 1 g, dávka takrolimu se snižuje tak, aby sérová koncentrace byla menší než 6 ng/ml. Koncentrace cyklosporinu by měla být nižší než 150 ng/ml. Kortikosteroidy se ponechávají ve zvýšené dávce, obvykle 20 mg denně. Při těžké infekci se imunosupresivní medikace přeruší na 8–10 dní podle závažnosti onemocnění a podává se pouze kortikosteroid. Pacienti s těžkou infekcí nebo se septickým šokem mohou mít relativní insuficienci nadledvin a je u nich indikováno podání stresové dávky kortikosteroidů (hydrokortizon v dávce 400 mg i.v.).9
Některá antibiotika mohou ovlivňovat sérové koncentrace imunosupresiv. Ovlivněny jsou především kalcineurinové inhibitory, které podléhají celé řadě lékových interakcí. Ze skupiny antimikrobních látek, které ovlivňují koncentrace cyklosporinu a takrolimu, je třeba zmínit především makrolidová antibiotika (klaritromycin – Klacid, Fromilid, azitromycin – Sumamed, Azitrox – a v menší míře roxithromycin), dále je to metronidazol (Entizol) a azolová antimykotika (itrakonazol – Sporanox – a ve vyšších dávkách i flukonazol – Mycomax).10 Tato antimikrobní léčiva mohou výrazně zvýšit koncentrace kalcineurinových inhibitorů, takže může dojít k projevům toxicity, včetně rozvoje nefrotoxicity. Naopak rifampicin (Benemycin) urychluje odbourávání cyklosporinu i takrolimu, a může tak dojít k rejekci transplantovaného orgánu nebo ke vzplanutí autoimunitní choroby.11 Z méně běžných antiinfektiv pak mají velký interakční potenciál antivirotika v terapii HIV a hepatitidy C.
U pacientů je třeba rovněž kontrolovat chronicky podávanou medikaci, která může ovlivnit vstřebávání antibiotik. Vazače fosfátů (sevelamer – Renagel, Renvela, lanthan karbonát Fosrenol, případně vazače na bázi železa – Velphoro), stejně jako kalcium, které se podává jako prevence steroidní osteoporózy, magnezium a železo snižují vstřebání ciprofloxacinu a doxycyklinu. Společné podání azathioprinu a kombinace trimetoprim/sulfametoxazolu (Cotrimoxazol, Biseptol) zvyšuje riziko neutropenie. Všechna antibiotika mohou způsobit střevní dysmikrobii s následným poklesem produkce vitaminu K střevní mikroflórou. U warfarinizovaného pacienta tak může dojít k výraznému vzestupu mezinárodního normalizovaného poměru (INR) a ke krvácení. Nejčastěji se tento problém vyskytuje po podání běžných širokospektrých penicilinů (např. amoxicilin/klavulanát – Augmentin, Amoksiklav), ale rizikové je i podání cefalosporinů, makrolidových antibiotik, klindamycinu (Dalacin), chinolonů a dalších. Při akutní infekci přerušujeme léčbu přípravky železa. Podávání léků stimulujících erytropoézu (erytropoetin, darbepoetin) při infekci nepřerušujeme, ale dávku nezvyšujeme, i když jejich účinnost při infekci klesá.12
Dávkování antibiotik při hemodialýze závisí na tom, zda má pacient reziduální diurézu, i když není zcela podmínkou, že zachovaná reziduální diuréza je vždy spojena se zachovanou eliminační schopností ledvin. Dále je důležité vědět, zda se podávané antibiotikum metabolizuje v játrech, nebo se odstraňuje renálně, a zda tedy bude při renální insuficienci významně ovlivněna jeho farmakokinetika. Lék, který se odstraňuje při hemodialýze, se musí podat v substituční dávce po ukončení dialýzy. Účinnost dialýzy na odstraňování antibiotika závisí na jeho vazbě na plazmatické bílkoviny a na jeho distribučním objemu (velký distribuční objem znamená malou efektivitu dialýzy). Z hlediska dialyzační léčby záleží na délce a frekvenci dialyzační procedury. Lékař v hemodialyzačním středisku by měl být o podávání antibiotika informován, aby mohl eventuálně dávkování léku upravit. Peritoneální dialýza je metoda, kdy jsou látky z organismu odstraňovány kontinuálně, nicméně daleko pomaleji než v průběhu hemodialyzační procedury. Antibiotikum se podává dle reziduální diurézy a dávka se redukuje v závislosti na eliminaci podávaného léku (renální, nebo hepatální vylučování).13 U peritoneálně dialyzovaných pacientů se při peritonitidě podávají antibiotika intraperitoneálně.
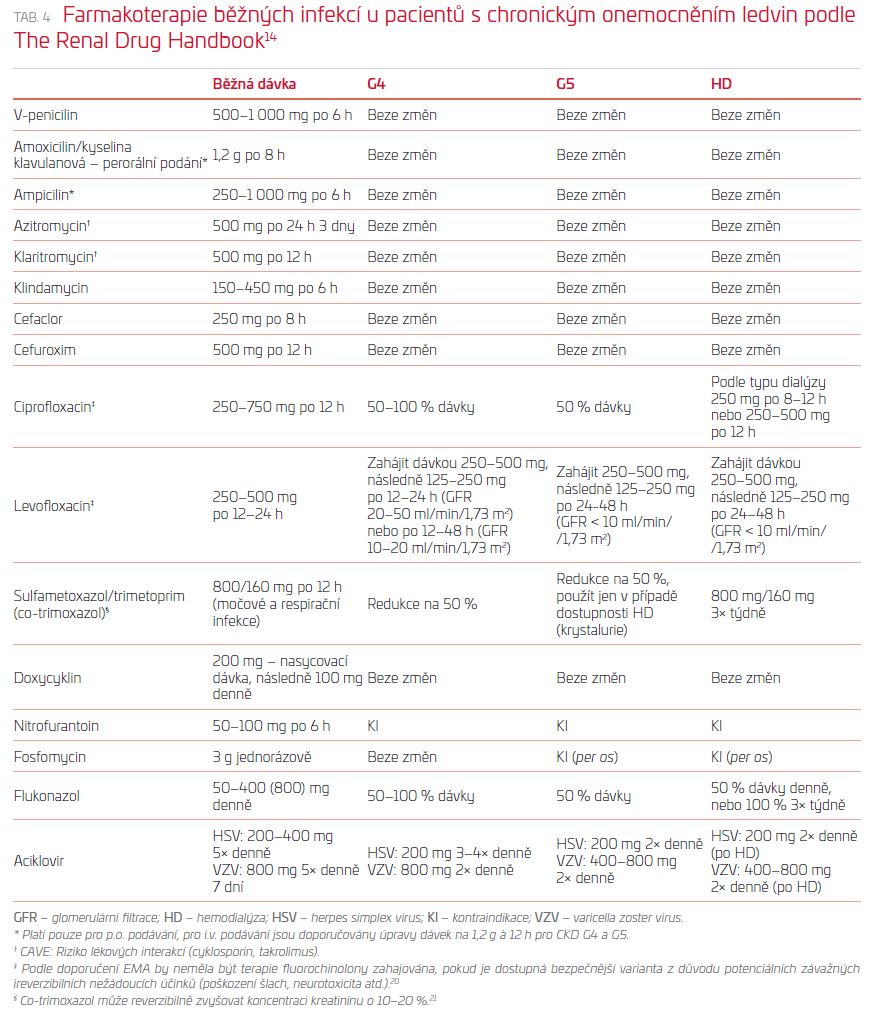
Dávka antibiotik vylučovaných renálně u pacientů s chronickým onemocněním ledvin se upravuje podle velikosti glomerulární filtrace. Jako obecné pravidlo může sloužit doporučení, že ve stadiu G2–G3a se dávka antibiotika snižuje o 50–75 % a interval podávání zůstává beze změny a ve stadiu G3b– G4 se dávka snižuje na 50 % a interval se prodlužuje dvojnásobně. Ve stadiu G5 zůstává redukce dávky stejná, ale interval se u některých antibiotik prodlužuje. Různé zdroje se významně liší v doporučeních, jak redukovat dávky antibiotik při renální insuficienci, počínaje souhrny údajů o léčivém přípravku (SPC), jež podávají často alibistické informace a doporučují dramatické snižování dávek i u velice bezpečných látek, po doporučení z klinické praxe, která bývají často naopak poměrně benevolentní.14,15 Přehled doporučení pro perorálně podávaná antibiotika u pacientů s renální insuficiencí je uveden v tabulce 4.14
Při rozvaze o úpravě dávek je třeba si rovněž uvědomit, že antibiotika zpravidla podáváme pouze krátkou dobu a patří mezi ně látky s diametrálně odlišným bezpečnostním profilem. I když peniciliny a cefalosporiny jsou vylučovány v naprosté většině především renálně, a jejich farmakokinetika je tedy renální insuficiencí významně ovlivněna, jedná se o natolik bezpečné léky, že můžeme být v redukcích dávek méně striktní. Látky, které vyžadují významné snížení dávek, jsou potom spíše rezervovány pro parenterální použití za hospitalizace (vankomycin, aminoglykosidy). Jako příklad z klinické praxe nám může posloužit porovnání amoxicilinu/klavulanátu a ciprofloxacinu. Clearance amoxicilinu klesá u pacientů léčených hemodialýzou asi desetkrát a u kyseliny klavulanové je to přibližně 3,5krát.16 V případě ciprofloxacinu klesá clearance přibližně o 50 %.17 Přestože vliv renální insuficience je významnější v případě aminopenicilinu, recentní doporučení uvádějí vzhledem k dobrému bezpečnostnímu profilu možnost jeho podávání per os bez úpravy dávek. Naopak dávky ciprofloxacinu se snižují pro možný rozvoj NÚ (tab. 4).14 V případě vyšších dávek amoxicilinu se ojediněle vyskytují případy krystalurie, které mohou dále poškodit ledviny, tento nežádoucí účinek se rozvíjí především u pacientů se zakoncentrovanou močí s nízkým pH.18 Na tomto místě si dovolujeme upozornit, že dávkování léčiv u pacientů s poškozenými eliminačními funkcemi je jedním z problémů, se kterým může pomoci klinický farmaceut nebo farmakolog. Česká odborná společnost klinické farmacie ČLS JEP zahajuje projekt (ČOSKF) vybudování sítě informačních center v rámci stávajících oddělení klinické farmacie pro praktické lékaře v jednotlivých krajích, kam bude možné se s podobnými dotazy obrátit.
Preventivní podání antibiotik je indikováno u dialyzovaných a imunosuprimovaných pacientů při chirurgických výkonech. Při stomatologickém výkonu je indikován amoxicilin/klavulanát nebo klindamycin, při výkonu v urogenitální oblasti pak amikacin s ampicilinem nebo metronidazol. Založení arteriovenózní píštěle se provádí v antibiotické cloně. Podává se amoxicilin/klavulanát nebo klindamycin. Implantace peritoneálního katétru je pokryta cefalosporinem 1. generace. Imunosuprimovaní pacienti užívají preventivně pro riziko pneumocystové pneumonie trimetoprim/sulfametoxazol. Součástí imunosupresivních schémat je antivirová a antimykotická profylaxe.19 Z azolových antimykotik je renální insuficiencí nejvíce ovlivněn flukonazol (Mycomax), jehož poločas se výrazně prodlužuje, a je doporučeno při závažné renální insuficienci snižovat dávky na 50 %. Rovněž dávky acikloviru (Zovirax, Herpesin) je třeba snižovat (tab. 4).
Pacienti s chronickým onemocněním ledvin jsou ohroženi zvýšeným rizikem infekcí a léčba je ovlivněna stupněm renální insuficience a způsobem vedení terapie u dialyzovaných pacientů. Nemocní, kteří jsou pro své základní renální onemocnění léčeni kombinovanou imunosupresivní léčbou, představují samostatnou skupinu pacientů, u kterých je léčba velmi obtížná, často musí být imunosupresivní medikace vysazena, což velmi nepříznivě ovlivňuje jejich prognózu, v případě pacientů po transplantaci funkci štěpu.
Literatura
- KDIGO 2012 Clinical Practice Guideline for the Evaluation and Management of Chronic Kidney Disease. Kidney Int 2013;3:1–150.
- Clinical Practice Guidelines on management of older patients with chronic kidney disease stage 3b or higher (eGFR ≤ 45 ml/min). Nephrol Dial Transplant 2017;32:9–16.
- KDIGO Clinical Practice Guideline for Glomerulonephritis. Kidney Int Suppl 2012;2:139–274.
- Bertrand J. Bacterial infections in hemodialysis patients: Pathogenesis and prevention. Principal discussant. Kidney Int 2005;67:2508–2519.
- NKF‑KDOQI Clinical Practice guidelines for Vascular Access: Update 2006. Am J Kidney Dis 2006;48:S248–272.
- Rychlík I, Lopot F. Statistická ročenka ČNS 2017.
- Li PK, Szeto C, Piraino B, et al. ISPD guidelines Recommendations: 2016 update on prevention and treatment. Perit Dial Int 2016;36:481–508.
- Ntatsaki E, Carruthers D, Chakravarty K, et al. BSR and BHPR guidelines for the management of adults with ANCA‑associated vasculitis. Rheumatology 2014;53:2306–2309.
- Alangaden GJ, Thyagarajan R, Gruber SA, et al. Infectious complications after kidney transplantation: current epidemiology and associated risk factors. Clin Transplant 2006;20:401–409.
- Nara M, Takahashi N, Miura M, et al. Effect of itraconazole on the concentrations of tacrolimus and cyclosporine in the blood of patients receiving allogeneic hematopoietic stem cell transplants. Eur J Clin Pharmacol 2013;69:1321–1329.
- Sadaba B, Lopez de Ocariz A, Azanza JR, et al. Concurrent clarithromycin and cyclosporin A treatment. J Antimicrob Chemother 1998;42:393–395.
- Teehan G, RuthazerR, Balakrishnan V, et al. Iron storage indices and risk of bacterial infections in hemodialysis patients. Hemodialysis Int 2004;24:226–232.
- Dusilová‑Sulková S. Aktuální otázky bezpečnosti farmakoterapie u pacientů s chronickým onemocněním ledvin. Postgraduální nefrologie 2015;13:52–54.
- Ashley C, Dulneway A. The Renal Drug Handbook, 5. vydání, 2019, CRC Press, Taylor & Francis Group.
- Smyth B, Jones C, Saunders J. Prescribing for patients on dialysis. Aust Prescr 2016;39:21–24.
- Horber FF, Frey FJ, Descoeudres C, et al. Differential effect of impaired renal function on the kinetics of clavulanic acid and amoxicillin. Antimicrob Agents Chemother 1986;29:614–619.
- Gasser TC, Ebert SC, Graversen PH, et al. Ciprofloxacin pharmacokinetics in patients with normal and impaired renal function. Antimicrob Agents Chemother 1987;31:709–712.
- Hentzien M, Lambert D, Limelette A, et al. Macroscopic amoxicillin crystalluria. Lancet 2015;385:2296.
- Antimicrobial Treatment Guidelines for Common Infections 2016, The NB Provincial Health Authorities Anti‑infective Stewardship Committee under the direction of the Drugs and Therapeutics Committee.
- Disabling and potentially permanent side effects lead to suspension or restrictions of quinolone and fluoroquinolone antibiotics, 11 March 2019, EMA/175398/2019.
- Dijkmans BA, van Hooff JP, de Wolff FA, Mattie H. The Effect of co‑trimoxazole on serum creatinine. Br J Clin Pharmacol 1981;12:701–703.
- Kategorie: Přehledové články
- Klíčová slova: antibiotická léčba; hemodialyzační léčba; chronické onemocnění ledvin; imunosupresivní léčba; peritoneální dialýza; transplantace ledvin