Vakcinace u pacientů s onemocněním ledvin a po transplantaci
Infekční komplikace jsou jedněmi z nejčastějších komplikací u pacientů s chronickým onemocněním ledvin (CKD).1 Ve srovnání s obecnou populací se infekce u pacientů s CKD vyskytují častěji, mají závažnější a protrahovaný průběh s vyšším rizikem úmrtí. Samotná infekce může dále vést k dekompenzaci základního onemocnění, např. k progresi do nezvratného selhání ledvin, ke zhoršení ischemické choroby srdeční, chronického srdečního selhání, diabetes mellitus (DM).2 Zvýšené riziko infekce je u pacientů s renálním onemocněním dáno imunokompromitovaným až imunosuprimovaným stavem. K oslabení imunitního systému přispívá uremie, anémie, vyšší věk spojený s oslabenou výkonností imunitního systému, hypoalbuminemie při malnutrici, nefrotickém syndromu, jiná závažná přidružená onemocnění (např. DM), ale i samotná hemodialýza či opakovaný pobyt ve zdravotnických zařízeních.3
Některým z infekčních onemocnění lze předcházet vakcinací. Přestože pacienti s onemocněním ledvin a po transplantaci jsou mnohem více náchylní k infekcím, a patří proto mezi prioritní z hlediska očkování, podstatné množství těchto pacientů zůstává neočkováno.4,5 Takto nechránění pacienti jsou kromě závažného rizika potenciálně smrtelné infekce vystaveni i riziku rejekce a ztráty transplantované ledviny. Očkovaní pacienti mají naopak významně lepší přežití.6
K nízké míře proočkovanosti jistě přispívají i mýty, které o očkování kolují. Pacienti, ale i odborná veřejnost se domnívají, že očkování (nejen) v populaci s CKD a po transplantaci nefunguje a pacienty před nákazou neochrání. Je pravda, že tito pacienti ve srovnání s obecnou populací dosahují nižší postvakcinační ochrany. Očkování u nich vede k nižší sérokonverzi, nižším absolutním koncentracím protilátek v séru, které rychleji klesají v čase. Navíc u této specifické populace chybějí dostatečné údaje o trvání postvakcinační ochrany.7
Šance na účinnou postvakcinační odpověď klesá s věkem, s progresí renální dysfunkce, je závislá na míře imunosupresivní léčby, zejména na dávce mykofenolát mofetilu.8–10 Proto by očkování mělo být zahájeno v časném stadiu chronického onemocnění ledvin. Po transplantaci nebyl interval jednoznačně stanoven, obecně se doporučuje s očkováním počkat tři až šest měsíců do ustálení imunosupresivní léčby. V případě hrozící epidemie či začátku sezony chřipky je možné očkovat i jeden měsíc po transplantaci. Očkování neživou vakcínou příliš časně po transplantaci nepředstavuje pro pacienta riziko infekce, může ale vést ke slabší a méně účinné postvakcinační odpovědi a k riziku nedostatečné séroprotekce. Po aplikaci rituximabu by se očkování mělo odložit o šest měsíců.
Postvakcinační ochrana obvykle nastupuje po dvou týdnech, dosahuje svého maxima jeden až tři měsíce po očkování, přetrvává minimálně šest měsíců (v případě chřipky). U očkování s dobrou korelací mezi séroprotektivní koncentrací protilátek a skutečnou postvakcinační ochranou (např. tetanus, hepatitida B, klíšťová encefalitida) se doporučuje v odstupu minimálně čtyř týdnů, ideálně dvou měsíců, zhodnotit bezprostřední či dlouhodobou postvakcinační imunitu sérologickým vyšetřením.
Mezi nástroje, jak obecně zvýšit šanci na účinnou postvakcinační odpověď, patří vyšší dávka vakcíny, přídatná dávka (tzv. booster), použití adjuvantní vakcíny či intradermální podání. U pacientů po transplantaci ledviny se v případě očkování proti chřipce prokázaly jako účinné první dva uvedené způsoby, tj. vyšší dávka vakcíny nebo booster.11 Vzhledem k nižší odpovědi na očkování u pacientů s CKD by měly být očkovány i osoby blízké, žijící ve společné domácnosti a ošetřující zdravotnický personál, u kterých se předpokládá dobrá odpověď na očkování a vytvoření pomyslného ochranného zámotku kolem nechráněných osob.
Ačkoliv se v minulosti objevily obavy ohledně zvýšené T lymfocytární reaktivity a novotvorby HLA protilátek po očkování, v současné době pro toto neexistují žádné relevantní klinické údaje a očkování není spojeno s rizikem odhojení transplantovaného orgánu. Naopak, vakcinace snižuje morbiditu a mortalitu v transplantované populaci.12
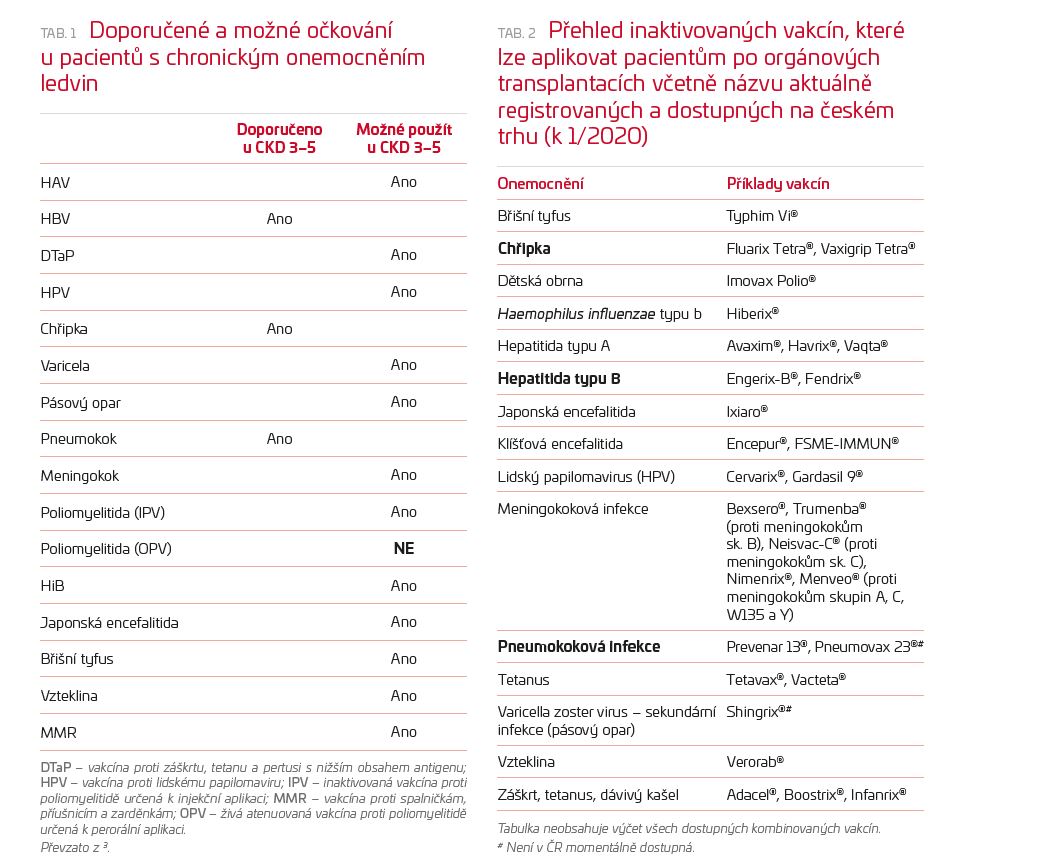
Doporučené a možné očkování u pacientů s chronickým onemocněním ledvin shrnuje tabulka 1. Mezi základní patří očkování proti pneumokokovým onemocněním, virové hepatitidě typu B (HBV), chřipce, varicele.
Pacienty po transplantaci ledviny podstupující imunosupresivní léčbu je možné očkovat pouze inaktivovanými, tj. neživými vakcínami dle doporučení pro obecnou populaci.13 Přehled inaktivovaných vakcín vhodných pro toto použití je uveden v tabulce 2. Při výběru očkovací látky je třeba postupovat individuálně, ideálně ve spolupráci s očkovacím a transplantačním centrem.
Po transplantaci jsou kontraindikovány živé oslabené vakcíny pro riziko replikace a diseminace onemocnění (tab. 3). U kandidátů transplantace se doporučuje očkovat před samotnou transplantací a dodržet minimálně dvoutýdenní odstup mezi aplikací živé vakcíny a samotnou transplantací, ideální doba je měsíc.14 Pokud by byla živá vakcína aplikována nedopatřením, doporučuje se podat specifickou antivirovou terapii (např. oseltamivir v případě očkování živou intranazální vakcínou proti chřipce) a následně očkovat neživou alternativou vakcíny.15
Chřipka
Onemocnění chřipkou zásadně zvyšuje morbiditu a mortalitu pacientů s CKD a po transplantaci a prostřednictvím přímých i nepřímých imunitních mechanismů zvyšuje riziko rejekce transplantovaného orgánu. U těchto pacientů se doporučuje každoroční očkování proti chřipce, ideálně před předpokládaným začátkem chřipkové sezony. Je možné očkovat už měsíc po transplantaci. Preferuje se intramuskulární podání standardní dávky tetravalentní inaktivované štěpené vakcíny (např. Vaxigrip Tetra®).
Pneumokok
Hlavními obávanými projevy infekce Streptococcus pneumoniae jsou tzv. invazivní pneumokoková onemocnění jako pneumonie, meningitida, sepse. Pneumokokové onemocnění často komplikuje chřipku, proto se u neočkovaných pacientů doporučuje při vakcinaci proti chřipce současné podání pneumokokové vakcíny jako prevence rozvoje superinfekce. K tomu slouží 13valentní konjugovaná vakcína (Prevenar 13®) a 23valentní polysacharidová vakcína (momentálně není v ČR dostupná).
Hepatitida B
Ideální doba pro podání vakcíny proti hepatitidě B je co nejdříve v průběhu chronického onemocnění ledvin z důvodu větší šance na efektivní postvakcinační imunitní odpověď. Doporučené schéma dávkování je 20 mg, tj. 1 ml nultý, první, šestý měsíc. Pacienti s pokročilou poruchou funkce ledvin mají sníženou imunitní odpověď na vakcínu proti hepatitidě B, proto se k zajištění dostatečné tvorby ochranných protilátek u pacientů v predialýze nebo léčených dialýzou doporučuje použití adjuvantní vakcíny, přidání jedné dávky ve druhém měsíci a navýšení dávky antigenu (tj. podání vakcíny Fendrix®, 40 mg, tj. 2 ml, schéma nultý, první, druhý, šestý měsíc). Po šesti až osmi týdnech dokončeného schématu očkovaní je potřeba provést sérologickou kontrolu anti‑HBs protilátek. Minimální protektivní koncentrace je 10 mIU/ml. Pokud pacient po aplikaci základního schématu této koncentrace nedosáhne, je nutné celé očkovací schéma aplikovat znovu. V případě, že se koncentrace protilátek pohybuje mezi 10–100 mIU/ml, aplikuje se jedna booster dávka. Pokud pacient nevytvoří protilátky ani po druhém očkovacím schématu, je označen za non‑respondéra a další očkování se již neprovádí.
U dialyzovaných pacientů se provádí pravidelná kontrola anti‑HBs protilátek jednou za dva až tři měsíce. Při poklesu hodnoty protilátek pod 100 mIU/ml již nelze zaručit dlouhodobou ochranu, a proto je vhodné podat booster dávku a dále vyšetřovat anti‑HBs protilátky jedenkrát ročně. Některá doporučení se v tomto liší a doporučují aplikaci booster dávky až při poklesu pod 10 mIU/ml.
Po transplantaci vykazují protektivní koncentrace anti‑HBs protilátek rychlý pokles, doporučuje se proto provádět sérologickou kontrolu každých 6 až 12 měsíců. V případě nedostatečné ochranné koncentrace protilátek (< 10 mIU/ml) je potřebná revakcinace posilující dávkou a opětovná kontrola anti‑HBs protilátek. Dle doporučení KDIGO (Kidney Disease: Improving Global Outcomes) je vhodné u pacientů po transplantaci ledviny zajistit přeočkování již při poklesu koncentrace anti‑HBs pod 100 mIU/ml z důvodu výhledového rychlého poklesu ochranných protilátek.16
Meningokok
Očkování proti meningokokovi je doporučováno u pacientů s CKD a po transplantaci ledviny s porušenou nebo zaniklou funkcí sleziny (hyposplenismem/asplenií), poruchou/deficitem komplementu a před zahájením léčby ekulizumabem. K očkování je nejběžněji používána konjugovaná tetravakcína (MCV4) proti čtyřem séroskupinám – A, C, W‑135, Y (Nimenrix®, Menveo®). Konjugovaná tetravakcína je z dostupných vakcín pro zajištění co nejširší dostupné ochrany nejvhodnější. Další zaregistrovanou vakcínou je rekombinantní čtyřkomponentní vakcína proti séroskupině B, vakcína MenB (Bexsero®, Trumenba®), která pokryje 74 % všech meningokoků skupiny B v ČR. Doporučuje se kombinace obou vakcín v odstupu minimálně 14 dní, v případě potřeby lze vakcíny aplikovat současně, avšak do odlišných míst na těle. K udržení dlouhodobé imunity je doporučeno u obou vakcín přeočkování, u MCV4 v pětiletých intervalech, u MenB nebyl interval přeočkování dospělých pacientů zatím stanoven.
Tetanus
Imunizace proti tetanu by měla být aktualizována podle obecných doporučení pro dospělou populaci. Očkování inaktivovanou vakcínou proti tetanu na bázi toxoidu je dostatečně imunogenní a bezpečné i v transplantované populaci.
Varicella zoster virus (VZV)
Pásový opar je častou komplikací po transplantaci ledviny. V průběhu sedmi let se pásový opar vyvine u 10 % pacientů, z toho 20 % z nich trpí postherpetickou neuralgií.17 Vakcína proti VZV je schopna podstatně snížit riziko těchto komplikací. Živá vakcína (Zostavax®), která byla po transplantaci kontraindikována, ale bylo možné ji aplikovat u kandidátů transplantace minimálně dva týdny před výkonem, není již v současné době na českém trhu dostupná. V budoucnu bychom mohli očekávat širší dostupnost již registrované neživé subjednotkové rekombinantní vakcíny proti VZV (Shingrix®) vhodné i pro pacienty podstupující imunosupresivní léčbu.
Shrnutí
Očkování představuje bezpečný a účinný způsob, jak u pacientů s onemocněním ledvin zásadně snížit riziko infekce a přidružených komplikací, dekompenzace základního onemocnění, ztráty transplantovaného orgánu a úmrtí. Vakcinační anamnéza, kontrola postvakcinační ochrany a vytvoření vakcinačního plánu by měly být součástí vyšetření před transplantací ledviny. Cesta ke zlepšení nízké proočkovanosti populace s CKD vede přes důslednou edukaci pacientů i zdravotníků a vyvracení mýtů. K zajištění efektivity je vhodné očkování plánovat na období před transplantací, ideálně do časného stadia chronického onemocnění ledvin, po transplantaci ledviny počkat na ustálení imunosupresivní léčby.
Literatura
- Naqvi SB, Collins AJ. Infectious complications in chronic kidney disease. Adv Chronic Kidney Dis 2006;13:199–204.
- Cheikh Hassan HI, Tang M, Djurdjev O, et al. Infection in advanced chronic kidney disease leads to increased risk of cardiovascular events, end‑stage kidney disease and mortality. Kidney Int 2016;90:897–904.
- Chlíbek R. Očkování hemodialyzovaných osob a pacientů s chronickým renálním selháváním. In: Chlíbek R (Ed.). Očkování dospělých. Praha: Mladá fronta, 2018.
- Bond TC, Patel PR, Krisher J, et al. Association of standing‑order policies with vaccination rates in dialysis clinics: a US‑based cross‑sectional study. Am J Kidney Dis 2009;54:86–94.
- Lee DH, Boyle SM, Malat G, et al. Low rates of vaccination in listed kidney transplant candidates. Transpl Infect Dis 2016;18:155–159.
- Bond TC, Spaulding AC, Krisher J, McClellan W. Mortality of dialysis patients according to influenza and pneumococcal vaccination status. Am J Kidney Dis 2012;60:959–965.
- Remschmidt C, Wichmann O, Harder T. Influenza vaccination in patients with end‑stage renal disease: systematic review and assessment of quality of evidence related to vaccine efficacy, effectiveness, and safety. BMC Med 2014;12:244.
- DaRoza G, Loewen A, Djurdjev O, et al. Stage of chronic kidney disease predicts seroconversion after hepatitis B immunization: earlier is better. Am J Kidney Dis 2003;42:1184–1192.
- Kumar D, Campbell P, Hoschler K, et al. Randomized Controlled Trial of Adjuvanted Versus Nonadjuvanted Influenza Vaccine in Kidney Transplant Recipients. Transplantation 2016;100:662–669.
- Scharpe J, Evenepoel P, Maes B, et al. Influenza vaccination is efficacious and safe in renal transplant recipients. Am J Transplant 2008;8:332–337.
- Hirzel C, Kumar D. Influenza vaccine strategies for solid organ transplant recipients. Curr Opin Infect Dis 2018;31:309–315.
- Mulley WR, Dendle C, Ling JEH, Knight SR. Does vaccination in solid‑organ transplant recipients result in adverse immunologic sequelae? A systematic review and meta‑analysis. J Heart Lung Transpl 2018;37:844–852.
- Kidney Disease: Improving Global Outcomes Transplant Work G. KDIGO clinical practice guideline for the care of kidney transplant recipients. Am J Transplant 2009;9(Suppl. 3):S1–S155.
- Kotton CN. Immunization after kidney transplantation – what is necessary and what is safe? Nat Rev Nephrol 2014;10:555–562.
- Danziger‑Isakov L, Kumar D, Practice ASTIDCo. Vaccination in solid organ transplantation. Am J Transplant 2013;13(Suppl. 4):311–317.
- Levitsky J, Doucette K, Practice ASTIDCo. Viral hepatitis in solid organ transplantation. Am J Transplant 2013;13(Suppl. 4):147–168.
- Zuckerman RA, Limaye AP. Varicella zoster virus (VZV) and herpes simplex virus (HSV) in solid organ transplant patients. Am J Transplant 2013;13(Suppl. 3):55–66; quiz 66.
- web České vakcinologické společnosti ČLS JEP: www.vakcinace.eu.
- Kategorie: Pacient s onemocněním ledvin v ordinaci ambulantního specialisty
- Klíčová slova: chronické onemocnění ledvin; inaktivované vakcíny; očkování; transplantace ledvin