Historie umělé ledviny ve světě
Souhrn
V roce 2025 uplynulo 80 let od první úspěšné klinické hemodialýzy pomocí umělé ledviny ve světě, v České republice byl tento výkon poprvé proveden o 10 let později. Ve Spojených státech amerických se používaly především Kolffovy umělé ledviny, v Evropě pak Alwallovy – v roce 1955 jich bylo pět: v Lundu, Hamburgu, Vídni, Curychu a v Praze. Další rozvoj léčby umělou ledvinou nastal v 60. letech minulého století a souvisí s vytvořením trvalých cévních přístupů, které umožňovaly opakované napojení pacienta na umělou ledvinu (Scribnerův shunt v roce 1960 a arteriovenózní fistule Cimino–Brescia–Appell v roce 1965). V dalších letech vznikaly kvalitnější umělé ledviny, dialyzátory, dialyzační roztoky, a nakonec i nové metody – dnes dominující hemodiafiltrace. Od konce 60. let minulého století se hemodialýza rozšířila i na pacienty s chronickým selháním ledvin budováním hemodialyzačních středisek v různých zemích světa, s rozdílnou dostupností péče. Dominantní zůstávají dodnes USA a Japonsko s prevalencí > 1 000 pacientů / 1 milion obyvatel, naopak chudé státy Afriky mají prevalenci < 100. Ve světě závisí rozvoj dialyzační léčby na ekonomickém stavu země a financování systému zdravotnictví.
Klíčová slova: hemodialýza – domácí hemodialýza – transplantace ledvin – hemodiafiltrace – dialyzační technologie – dialyzační roztok
Jak to všechno začalo – historie umělé ledviny
Thomas Graham byl skotský chemik, který se stal známým ve 2. polovině 19. století jako „Father of dialysis“, protože popsal význam slova dialýza – fyzikálního jevu spočívajícího v oddělování látek o různé molekulové hmotnosti z roztoků pomocí semipermeabilní membrány dvěma transportními mechanismy: difuzí a filtrací (konvekcí). Tento princip se stal klíčovým konceptem umělé ledviny.
V roce 1913 vyšel v londýnských Times článek s názvem „An artificial kidney“, který představoval první krok do budoucnosti. Popisoval první dialyzační přístroj určený pro psa. Zhotovili jej Američané J. Abel, L. Rowntree a B. Turner a nazvali jej „vividifusion“. Psovi byla odebrána krev, která byla spolu s hirudinem vedena do celofánové trubice. Ta byla volně navinuta kolem bubnu ponořeného do roztoku soli a dextrózy a pomalu se otáčela. Z krve se tak odstraňovala močovina i další látky. Jejich práce položila základy budoucí léčby selhání ledvin.
Georg Haas (1886–1971), německý lékař z Giessenu, provedl na své umělé ledvině v roce 1924 první hemodialýzu. V dalších letech dialyzoval celkem 11 pacientů s uremií a vždy jim odebíral krev a převáděl ji do svého přístroje – umělé ledviny. Všichni pacienti však nakonec zemřeli. Při svých prvních pokusech použil hirudin jako antikoagulant, později ve 30. letech začal používat také heparin.
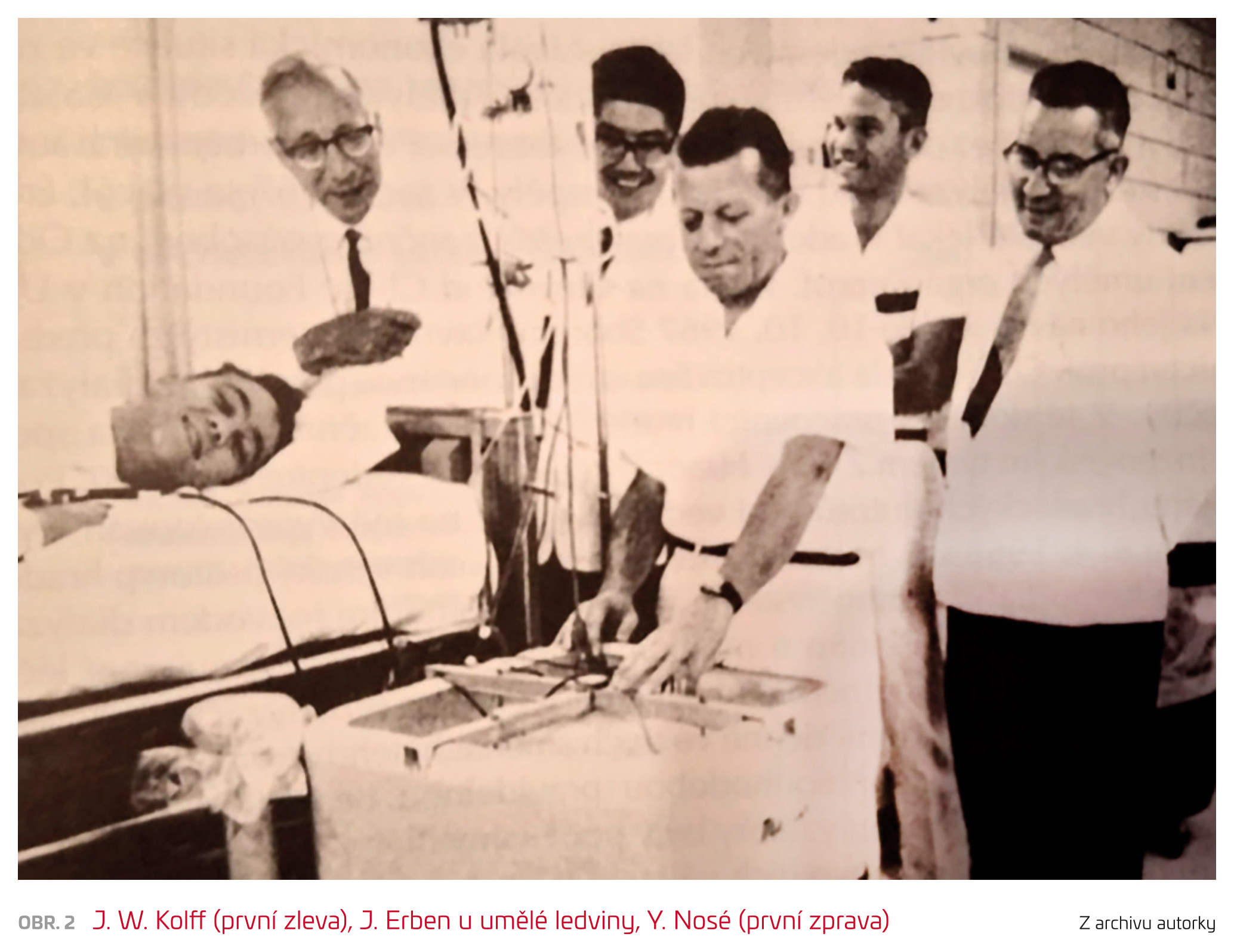
Skutečné průkopníky umělé ledviny ve světě ukazuje obrázek 1.
J. W. Kolff (1911–2009) byl holandský lékař, který v roce 1938 v univerzitní nemocnici v Groningenu přijal 22letého pacienta s uremií. Rozpoznal typické projevy tohoto onemocnění: extrémně vysoký krevní tlak, následnou ztrátu zraku, zažívací potíže a velmi vysoké hodnoty močoviny, kdy se její krystalky draly kůží ven a vyvolávaly úporné svědění. Pacient nakonec upadl do bezvědomí a krátce poté zemřel. Tato zkušenost byla pro Kolffa impulsem zabývat se možností technické náhrady funkce ledvin. Věděl o pokusech G. Haase i o americké „ledvině“ použité u psa a také o procesu dialýzy. Navštívil svého učitele biochemie profesora Brinkmana, který mu ukázal vhodný materiál pro experiment – německý celofán používaný jako střívko na výrobu párků. Kolff provedl jednoduchý pokus: 45 cm dlouhé celofánové „střívko“ uzavřel na obou koncích, naplnil jej 25 ml krve a přidal 100 mg močoviny. Trubici upevnil na desku, kterou ponořil do fyziologického roztoku a pohyboval s ní sem a tam. Po 15 minutách odebral z celofánové trubice vzorek a zjistil, že koncentrace močoviny je nulová. Byl překvapen a začal počítat: kdyby naplnil 10 m celofánové trubice 500 ml krve s močovinou a pohyboval jí ve fyziologickém roztoku, mohl by za 15 minut odstranit asi 2 g močoviny. Na základě těchto úvah začal sestavovat svůj přístroj – tzv. bubnovou ledvinu, v níž se válec s membránou otáčel v nádobě připomínající necky. V roce 1940 odešel do malé nemocnice v Kampenu, kde v místnosti ve sklepě pracoval již s malým týmem – dvěma sestrami, jednou laborantkou a medikem J. van Noordwijkem. V letech 1943–1945 zde dialyzoval 15 pacientů s chronickým selháním ledvin a pokročilou uremií. Všichni pacienti zemřeli, i když byly zaznamenány i přechodné momenty zlepšení klinického stavu a laboratorních hodnot. Přístroj si proto vysloužil přezdívku „smrtící stroj“. Kolff však věděl, že musí přístroj použít u pacienta s náhlým selháním ledvin, kde by mohl být úspěšnější.
Dne 3. září 1945 byla na chirurgické oddělení nemocnice přivezena z vězeňského tábora 67letá žena Sofie Schafstadtová s horečkou, žloutenkou, v bezvědomí a s krevním tlakem 250/160 mm Hg. Chirurg indikoval cholecystektomii, ale vzhledem k těžkému stavu pacientky zahájil léčbu sulfonamidy. Na konzilium byl opakovaně přizván dr. Kolff pro vysokou hodnotu močoviny (2 g/l). Dne 6. září horečka klesla a léčba sulfonamidy byla ukončena. Dne 9. září Kolff zjistil, že pacientka je v uremickém kómatu, a rozhodl se pokusit o léčbu pomocí umělé ledviny. Dne 11. září dosáhla koncentrace močoviny 4 g/l a byla zahájena dialýza. Ta trvala 11 hodin, během nichž krevní tlak klesl na 160/80 mm Hg a koncentrace močoviny se snížila na 1,2 g/l. Přístrojem proteklo přibližně 80 litrů krve. Kolff se obával dalšího zklamání, které již několikrát zažil. 12. září se však pacientka probrala z bezvědomí, objevila se diuréza, která rychle narůstala, a koncentrace močoviny dále klesala. Tento případ byl důkazem, že umělá ledvina může zachránit život pacientům s akutním selháním ledvin. Pacientka byla propuštěna z nemocnice i z vězení, žila u svého syna nedaleko Utrechtu a zemřela v roce 1951, tedy šest let po první hemodialýze.
Kolff se ve své vlasti nedočkal výrazného uznání ani pochvaly a svou umělou ledvinu si ani nenechal patentovat. Prvních pět přístrojů proto poslal do Haagu, Londýna, Amsterodamu, Krakova a New Yorku. V roce 1947 obdržel pozvání na konferenci v USA (Atlantic City), kde se někteří lékaři začali o jeho přístroj zajímat, včetně slavného nefrologa J. P. Merrilla. První hemodialýza v USA byla provedena v New Yorku až v roce 1948. Někteří američtí lékaři však byli k přístroji skeptičtí a tvrdili, že dlouhodobá náhrada funkce ledvin není možná. Přesto americké úřady v roce 1949 uznaly léčbu umělou ledvinou za standardní léčebnou metodu při selhání ledvin. Přístroj se významně osvědčil během války v Koreji (1950–1953), kdy úmrtnost vojáků po těžkých zraněních komplikovaných selháním ledvin klesla z 80 % na 50 %. Kolff se definitivně přesunul do USA v roce 1950 na kliniku v Clevelandu, kde umělou ledvinu dále zdokonaloval a vyrobil dalších 40 přístrojů, již z nerezové oceli. Na klinice mohl pacienty dialyzovat pouze v noci, po skončení ordinačních a operačních hodin.
Světového rozšíření však hemodialýza dosáhla až po zavedení Scribnerova zkratu v roce 1960, který umožnil opakované a relativně jednoduché napojení pacienta na umělou ledvinu. Díky tomu začala vznikat dialyzační střediska i pro pacienty s chronickým selháním ledvin.
Další významný rozvoj hemodialýzy nastal po roce 1966, kdy byla poprvé provedena arteriovenózní fistule cévním chirurgem C. Appelem na návrh interních lékařů M. Brescia a J. Cimina v nemocnici pro válečné veterány v Bronxu. Tento cévní přístup je dodnes považován za zlatý standard pro hemodialýzu.
Kolff je považován za jednoho z nejvýznamnějších lékařů 20. století a bývá označován jako „otec umělých orgánů“, jimž se v USA dlouhodobě věnoval. Byl oceněn 12 čestnými doktoráty a více než 120 mezinárodními oceněními. U profesora Kolffa se školilo mnoho lékařů nejen z USA, ale i z Evropy. Jedním z nich byl také MUDr. Josef Erben z Hradce Králové, pozdější profesor, který v roce 1966 absolvoval roční stáž v Clevelandu u „otce umělé ledviny“ na přímluvu profesora J. Broda (obr. 2).
Nils Alwall (1904–1986), švédský profesor Univerzity v Lundu, zhotovil také vlastní umělou ledvinu a dne 3. září 1946 úspěšně dialyzoval prvního pacienta s akutním selháním ledvin po dobu 6 hodin. Alwallova umělá ledvina byla konstrukčně odlišná od Kolffovy, protože dialyzační roztok v ní trvale protékal kolem navinuté dialyzační hadice s krví pacienta a současně umožňoval i ultrafiltraci. Alwall je považován za průkopníka také dalších metod, zejména izolované ultrafiltrace a hemofiltrace. Byl spoluzakladatelem firmy Gambro, jejíž dialyzační monitory byly velmi oblíbené i v České republice v 90. letech minulého století až do doby zániku společnosti. Prof. Alwall se často účastnil odborných akcí, mimo jiné i druhého mezinárodního nefrologického kongresu v Praze v roce 1963, který byl poprvé konán pod záštitou International Society of Nephrology.
Zajímavý byl případ jednoho jeho pacienta s nefrotickým syndromem, u něhož po dobu šesti týdnů prováděl izolovanou ultrafiltraci a odstranil tak přibližně 30 litrů tekutin. Alwall se také významně zasloužil o budování sítě hemodialyzačních středisek ve Švédsku – v roce 1972 jich bylo 19 a v roce 1982 již 32.
V historii umělé ledviny bývá uváděn ještě třetí průkopník – Gordon Murray z Kanady. Ten spolu se svým kolegou dr. Roschlauem vyvinul v 50. letech přístroj nazvaný „Murray–Roschlau artificial kidney“. Ještě před oznámením výsledků a podáním patentu však jeden z inženýrů z jeho týmu ukradl konstrukční návrhy a odešel do Německa, kde začal podobný přístroj vyrábět a prodávat. Původní autoři tak postupně upadli v zapomnění.
V 60. letech se objevil dialyzační monitor, jehož autorem byl norský urolog Fred Kiil (obr. 3). Přístroj měl podobu velké dialyzační desky s membránou z cuprophanu a nebylo u něj nutné používat krevní pumpu. Používal jej také B. H. Scribner v Seattlu a krátce byl zaveden i v Praze na II. interní klinice Všeobecné fakultní nemocnice. Kolff i Merrill však v té době preferovali především cívkové dialyzátory.

Technický vývoj dialýzy pokračoval i v dalších desetiletích. V 50. letech minulého století vznikly v USA dialyzační monitory společnosti Travenol podle Kolffa a Watschingera (1956), později vyráběné firmou Baxter Travenol (obr. 4 – první zleva v obou řadách). Tyto přístroje pracovaly ještě s recirkulačním systémem, kdy byl dialyzátor (cívka) ponořen v dialyzačním roztoku. Každou minutu však přitékalo přibližně 500 ml čerstvého dialyzačního roztoku a stejné množství přepadem odtékalo do odpadu. Tento typ dialyzačního monitoru byl od roku 1967 používán také v Československu, ve Všeobecné fakultní nemocnici v Praze na II. interní klinice dokonce až do roku 1987. Největší a nejtěžší součástí přístroje byla nádrž na dialyzační roztok o objemu 120 litrů, který se připravoval ze 4 litrů dialyzačního koncentrátu a 116 litrů vodovodní vody. Přístroj byl vybaven dialyzační i krevní pumpou a během hemodialýzy se kontinuálně podával heparin (20 000 IU v 500 ml fyziologického roztoku) po dobu 8–10 hodin. Tyto přístroje ještě neměly detektor vzduchu, a dialyzační sestry proto vizuálně kontrolovaly hladinu heparinového roztoku v infuzní láhvi, protože při nedostatečném průtoku krve do dialyzátoru si pumpa mohla nasát heparinový roztok a následně i vzduch, což představovalo riziko vzduchové embolie. Velké ultrafiltrace, například odstranění 4 litrů tekutin během hemodialýzy, bylo obtížné dosáhnout a často se provádělo zvýšením venózního tlaku pomocí tlačky nebo peánu. Bezpečnost hemodialýzy tak byla do značné míry závislá na zkušenostech dialyzačních sester a lékařů.
Do historie české dialyzační techniky patří také tzv. Hradecký systém, kdy pod vedením MUDr. Josefa Erbena a ve spolupráci s pracovníky ZVÚ (Závodů vítězného února) v Hradci Králové byl navržen dialyzační systém a uveden do provozu v roce 1968. Skládal se ze šesti monitorů s centrálním rozvodem dialyzačního roztoku a cívkovými dialyzátory. Denně bylo možné dialyzovat 12–18 pacientů, což v době velkého nedostatku dialyzační kapacity představovalo významný pokrok. Tento systém byl zaveden také do dalších zdravotnických zařízení, například v Plzni, Českých Budějovicích, Olomouci, Košicích i v tehdejší NDR.
Technický vývoj dialýzy ve světě postupoval rychleji než u nás, nicméně v současnosti jsou všechna hemodialyzační střediska v České republice vybavena moderní technikou. Dominují zde především dvě společnosti – B. Braun Avitum a Fresenius Medical Care. Moderní dialyzační monitory jsou řízeny počítačem, který podle zadaných údajů na začátku výkonu (délka dialýzy, krevní průtok, počáteční a cílová hmotnost pacienta a další parametry) automaticky řídí průběh hemodialýzy. Během výkonu lze kdykoli sledovat například křivku ultrafiltrace, hodnoty krevního tlaku či ukazatel dialyzační účinnosti Kt/V. Přístroje jsou vybaveny řadou bezpečnostních prvků, jako jsou snímače arteriálního a venózního tlaku, snímač vstupního tlaku před dialyzátorem pro detekci srážení krve, detektor vzduchových bublin a další alarmové systémy.
Pro obsluhující personál je dnes hemodialýza výrazně bezpečnější a technicky přehlednější. Přesto je nezbytné, aby byl dialyzační personál důkladně vyškolen pro rutinní provoz a aby byl na každém hemodialyzačním středisku k dispozici aktuální provozní manuál.
Dialyzátor
Dialyzátor je nejdůležitější součástí umělé ledviny, ve které probíhá vlastní očišťovací proces – dialýza. Od konce 60. let minulého století se používaly tři základní typy dialyzátorů: cívkový (coil), deskový a kapilární (obr. 5).

Cívkový dialyzátor vyvinuli v roce 1956 W. Kolff a B. Watschinger ve spolupráci s firmou Baxter. Měl plnicí objem přibližně 500 ml a zasouval se do kotlíkové nádoby v horní části dialyzačního monitoru. Kolem cívky přitékal dialyzační roztok rychlostí přibližně 500 ml/min a stejným množstvím opět odtékal (tzv. recirkulační systém). Dialyzační membránu tvořila přírodní celulóza označovaná jako cuprophan. Zpočátku k nám byly cívky pouze dováženy, od konce 60. let minulého století se však začaly vyrábět v pražské pobočce podniku Transport a později v Dalečíně, kde se ročně vyrábělo 60–70 tisíc kusů až do druhé poloviny 80. let. Tyto československé cívky však často vykazovaly nižší kvalitu a docházelo k častým rupturám dialyzační membrány. To vedlo k různě velkým ztrátám krve do dialyzačního roztoku a jediným řešením bylo ukončení hemodialýzy, výměna cívky a opětovné zahájení výkonu. Ztráty krve u pacientů mohly být značné a bylo nutné je rychle nahradit transfuzí erytrocytární masy, protože v té době byla u dialyzovaných pacientů běžná hodnota hematokritu kolem 20 %. Do měsíčních rozborů dialyzační léčby jsme na našem hemodialyzačním středisku zapisovali jak počet ruptur cívky, tak počet transfuzí.
Po období cívkových dialyzátorů následoval krátký přechod na československý deskový dialyzátor Chiraplat DD1 a DD2 (pro provoz náročný) a později i na menší typ Chiraplat DDJ (1985–1991) o rozměrech přibližně 5 cm × 5 cm × 25 cm. Deskový dialyzátor Gambro Lundia plate jsme na našem středisku používali jen výjimečně, zejména u pacientů s tendencí ke srážení krve v dialyzátoru a preventivně u pacientů v pooperačním stavu.
Kapilární dialyzátor, jehož autorem byl americký výzkumník R. Stewart (1964), je dodnes nejrozšířenějším typem dialyzátoru. Má výrazně menší plnicí objem, obvykle méně než 150 ml. Je dlouhý přibližně 25–30 cm a váží 200–300 g. Skládá se z pouzdra, ve kterém je uloženo několik tisíc kapilárních vláken o průměru 150–200 µm a tloušťce stěny přibližně 50 µm. Pokud bychom všechna tato vlákna spojili za sebou, jejich celková délka by dosahovala přibližně 1 km. Na obou koncích pouzdra jsou vstupy a výstupy pro krev i dialyzační roztok, který protéká mezi kapilárami v protisměru proti proudu krve.
Technický pokrok dialyzačních monitorů umožnil ve druhé polovině 70. let přechod na jednoprůtočný systém (single‑pass). V Československu se však začal používat později, zejména v 80. a především v 90. letech minulého století, spolu s dovozem dialyzačních monitorů firem Gambro (např. AK 10), Fresenius a dalších, a současně s dovozem kapilárních dialyzátorů. První používanou dialyzační membránou byl cuprophan, který nebyl optimálně biokompatibilní. Jeho dlouhodobé používání sice jen vzácně vyvolávalo alergické reakce, ale výrazně vedlo ke zvýšení koncentrace β2‑mikroglobulinu v krvi a u mnoha pacientů ke vzniku bolestivého syndromu karpálního tunelu, který často vyžadoval chirurgické řešení. V současnosti dominují syntetické membrány, především z polysulfonu, někdy s přídavkem polyvinylpyrrolidonu. V minulosti se používaly také membrány z polyamidu nebo polykarbonátu. Jednotlivé membrány se liší například permeabilitou, velikostí pórů, tloušťkou stěny, elektrickým nábojem a dalšími parametry. Dnes je k dispozici také membrána na bázi celulózy modifikované triacetátem, která se používá u pacientů alergických na syntetické membrány. Velmi důležitým parametrem je biokompatibilita membrány, tedy snášenlivost umělého materiálu s krví pacienta. Kontakt mezi krví a membránou v dialyzátoru nesmí vyvolat toxické, zánětlivé ani imunologické reakce. Nesnášenlivost materiálu se může projevit alergickou reakcí různé intenzity – zarudnutím, dušností nebo poklesem krevního tlaku. Nejzávažnější formou je tzv. first use syndrome, tedy šokový stav, který se může objevit při první hemodialýze nebo při změně dialyzátoru na typ s jinou membránou. Při zahájení hemodialýzy je proto vhodné začínat s nižším průtokem krve (méně než 100 ml/min) a během prvních 10 minut jej postupně zvyšovat.
Dialyzátory jsou dnes sterilizovány gama zářením nebo párou, dříve se používala sterilizace ethylenoxidem, který byl častým zdrojem alergických reakcí. Každý dialyzátor má svou technickou charakteristiku uvedenou v dokumentaci výrobce. Lékař, který dialyzátor pro pacienta vybírá, musí znát jeho základní parametry: typ membrány (včetně tloušťky stěny), velikost dialyzační plochy (0,5–2,3 m²), způsob sterilizace (pára, gama záření), plnicí objem (obvykle 100–150 ml) a ultrafiltrační koeficient (KUF), který se udává v ml/h.
Podle hodnoty KUF rozlišujeme dialyzátory:
- nízkopropustné (low flux) s KUF < 20 ml/h/mm Hg,
- vysokopropustné (high flux) s KUF ≥ 40 ml/h/mm Hg, používané zejména pro hemodiafiltraci.
Dalším důležitým parametrem je clearance, která vyjadřuje, jaký objem krve je po průtoku dialyzátorem za jednotku času očištěn od určité látky (např. močoviny, kreatininu, fosfátů nebo vitaminu B12). Udává se v ml/min. Obecně platí, že při potřebě vyšší ultrafiltrace volíme dialyzátory s vyšším KUF, zejména při hemodiafiltraci. Pokud nepožadujeme velkou ultrafiltraci, pak zvolíme dialyzátor typu low flux. Lékař musí těmto parametrům dobře rozumět, aby pro pacienta zvolil vhodný dialyzátor i optimální dialyzační metodu. U vysoce propustných membrán (např. Theralite nebo Theranova) byly popsány ztráty albuminu během hemodialýzy, proto výrobci doporučují pravidelnou kontrolu jeho hladiny. V současnosti se pro hemodiafiltraci používají převážně syntetické membrány v kombinaci s vysokým krevním průtokem (kolem 400 ml/min), což výrazně zvyšuje efektivitu dialyzační léčby.
Dialyzační roztok
Dialyzační roztok v počátcích hemodialýzy používal k úpravě acidobazické rovnováhy přímo bikarbonát. V polovině 60. let minulého století však začal dominovat acetátový koncentrát, který se v dialyzačním přístroji míchal s vodou. Návrat k bikarbonátovému dialyzačnímu roztoku byl podpořen zjištěním, že intradialyzační hypotenze nebo zvracení na konci hemodialýzy jsou často vyvolány zvýšenou hladinou acetátu v krvi pacienta. Acetát se totiž nestíhal dostatečně rychle přeměnit na bikarbonát, protože kapacita této metabolické přeměny je omezená. Současně bylo doporučeno používat pro přípravu dialyzačního roztoku kvalitní vodu upravenou reverzní osmózou, nikoli pouze vodu vodovodní. Tyto dvě změny samy o sobě významně zlepšily toleranci hemodialýzy u pacientů.
Další technické změny vedly k úpravám dialyzačních monitorů pro přípravu dialyzačního roztoku ze dvou složek: tzv. kyselé složky (koncentrát v barelech nebo plastových vacích) a bikarbonátového koncentrátu, který je dodáván v prášku nebo v plastovém obalu. Výsledný dialyzační roztok vzniká smícháním kvalitně upravené vody a těchto dvou koncentrátů. Jeho kvalita je během hemodialýzy kontrolována měřením vodivosti iontů, přičemž hlavním iontem je sodík. Koncentrace sodíku bývá nastavena přibližně na 140 mmol/l, s možností úpravy v rozmezí 120–145 mmol/l. Další ionty obsažené v kyselé složce mají v dialyzačním roztoku obvykle tyto koncentrace: draslík 0–4 mmol/l, vápník 1,25 mmol/l (někdy také 1,5 nebo 1,75 mmol/l), hořčík 0,25–0,75 mmol/l podle typu použitého koncentrátu. Glukóza je obvykle přítomna v koncentraci 5,5 mmol/l a výsledná koncentrace bikarbonátu se pohybuje přibližně mezi 32–36 mmol/l.
Dialyzační technika je v současné době na vysoké úrovni – je bezpečná, snadno ovladatelná a řízená počítačem. Přidané moduly, například pro přímo řízenou ultrafiltraci, profilování sodíku v dialyzačním roztoku, sledování parametru Kt/V nebo pro měření průtoku arteriovenózní fistulí metodou recirkulace, představují významný přínos pro zkvalitnění hemodialyzační léčby. Ne vždy však personál využívá všechny možnosti, které dialyzační monitor nabízí, k optimálnímu vedení hemodialýzy pacienta.
A jak to bylo dál – nové metody léčby selhání ledvin
Navzdory technologickému pokroku hemodialyzační terapie během několika desetiletí se tato metoda stále vyznačuje poměrně vysokou úmrtností a řadou různých komplikací. Proto se v dalších letech hledaly nové léčebné modality, mezi nimiž je jednou z nejvýznamnějších hemodiafiltrace, která je dnes široce používána.
V roce 1967 publikovali L. W. Henderson, A. Besarab a A. Michels článek „Blood purification by ultrafiltration and fluid replacement („diafiltration“)“, ve kterém představili novou metodu čištění krve založenou na velké ultrafiltraci současně s adekvátní náhradou tekutin. V této metodě se vhodně kombinují difuze a konvekce při použití vysoce propustné membrány, což zlepšuje odstraňování rozpuštěných látek v širokém spektru molekulových hmotností (uremických toxinů). Jde tedy o extrakorporální metodu náhrady funkce ledvin, která kombinuje principy hemodialýzy a hemofiltrace. Limitací této metody byla velká potřeba náhradního roztoku, který byl zpočátku podáván v infuzních lahvích a později ve vacích. Technický problém s náhradním roztokem byl zásadně vyřešen přístrojem Fresenius 5008 v roce 2005, který umožnil jeho přípravu přímo v dialyzačním přístroji. Současná technologie dnes umožňuje online produkci mikrobiologicky ultračisté tekutiny určené k reinfuzi, což výrazně zjednodušilo rutinní používání této metody. V literatuře byly popsány i další výhody hemodiafiltrace, například vyšší clearance močoviny, fosfátů, β2‑mikroglobulinu a dalších látek, stejně jako nižší výskyt intradialyzačních hypotenzí.
Dostupnost hemodiafiltrace ve světě je však různá. Přibližně 54 % pracovišť v Severní a Jižní Americe, Evropě, Asii a Austrálii tuto metodu používá, 28 % uvádí její nedostupnost a 18 % pracovišť na otázku neodpovědělo. Data z observačních studií navíc naznačují i pozitivní vliv této metody na délku přežití pacientů. Pro hemodiafiltraci je doporučován vyšší průtok krve, obvykle 300–400 ml/min, ve srovnání se standardní hemodialýzou, kde bývá přibližně 250 ml/min.
Zajímavá je také otázka výskytu stenóz arteriovenózní fistule při hemodiafiltraci ve srovnání s hemodialýzou. Studie provedená japonskými autory sledovala primární průchodnost arteriovenózní fistule po 24 měsících u dvou skupin pacientů (v každé skupině 87 pacientů).2 Výsledky ukázaly, že při léčbě hemodiafiltrací byla primární průchodnost arteriovenózní fistule zachována u 74,2 % pacientů, zatímco při hemodialýze pouze u 41,7 %. Autoři tento rozdíl vysvětlují tím, že hemodiafiltrace snižuje oxidační stres a zánětlivou aktivitu, čímž zlepšuje endoteliální funkci.
Hemofiltrace je metoda dnes využívaná především na jednotkách intenzivní péče. Původně byla prováděna jako kontinuální arteriovenózní hemofiltrace, dnes se používá především kontinuální venovenózní hemofiltrace. Tato metoda napodobuje glomerulární filtraci ledvin, ale neumožňuje tubulární resorpci, a proto je nutné ztrátu tekutin nahrazovat substitučním roztokem. Metoda odstraňuje vodu i malé a středně velké molekuly a je velmi dobře tolerována u hemodynamicky nestabilních pacientů, zejména u nemocných s nízkým krevním tlakem.
Indikace k zahájení této léčby se často shrnují pomocí akronymu AEIOU:
A – těžká acidóza,
E – elektrolytová dysbalance,
I – intoxikace,
O – objemové přetížení (overload),
U – uremie (např. s encefalopatií nebo perikarditidou).
Výhodou hemofiltrace oproti klasické hemodialýze je její pomalý a kontinuální průběh. Pacient může být na této metodě napojen několik dní i týdnů, takže léčba není časově omezena jako u hemodialýzy, která probíhá v několika hodinových sezeních.
Kde se začali dialyzovat první chronicky dialyzovaní pacienti a kdy se začalo s domácí hemodialýzou v USA
V roce 1960 působila v USA skupina významných osobností nefrologie, které zásadně přispěly k rozvoji dialyzační léčby. Patřili mezi ně W. Kolff a J. Merrill, kteří se vedle hemodialýzy věnovali také vývoji umělých orgánů a transplantaci ledvin. B. Scribner se zaměřoval především na technologii hemodialýzy a organizaci dialyzačních programů i následnou péči o dialyzované pacienty. Významnou osobností nefrologie byl rovněž G. E. Schreiner, avšak jeho role byla spíše na politické úrovni – zasazoval se o zajištění a rozšíření dostupnosti dialyzační léčby.3
Prvním chronickým pacientem léčeným hemodialýzou byl Clyde Shields v univerzitní nemocnici v Seattlu. První hemodialýza byla provedena 9. března 1960 a pacient zemřel po 11 letech léčby na infarkt myokardu. Druhý pacient zahájil hemodialýzu v dubnu 1960, v roce 1968 podstoupil úspěšnou transplantaci ledviny a zemřel po 28 letech od zahájení dialyzační léčby, rovněž na infarkt myokardu během golfového turnaje. Třetí pacient zahájil hemodialýzu v květnu 1960 a zemřel po 14 letech léčby na srdeční onemocnění. Tito tři pacienti byli pozváni jako čestní hosté na oslavu 10. výročí dialyzační léčby v Seattlu, kde se setkali s celým týmem, který o ně během let pečoval.
Domácí hemodialýza začala v roce 1960, kdy již byl vyřešen problém cévního přístupu díky zavedení Scribnerova shuntu. Pionýry této léčby byly čtyři skupiny lékařů: kolem B. Scribnera v Seattlu, J. Merrilla v Bostonu, S. Shaldona v Londýně a Y. Nosého v Japonsku. Díky tomu došlo k postupnému přesunu části pacientů z dialyzačních center do domácí péče. Domácí hemodialýza přinášela pacientům řadu výhod: léčbu v domácím prostředí, větší časovou nezávislost, možnost kratších, ale častějších dialyzačních výkonů, lepší laboratorní výsledky i celkový klinický stav. V té době byla navíc domácí dialýza také finančně výhodnější. Centrum v Seattlu v tomto směru ukazovalo ostatním pracovištím cestu a preferovalo domácí léčbu až u 90 % pacientů ve státě Washington.
V roce 1973 však došlo k návratu pacientů zpět do dialyzačních center, protože v USA byl spuštěn program Medicare pro pacienty s terminálním selháním ledvin. Dialyzační kapacita center se výrazně zvýšila a pacienti se postupně přesouvali z domácí péče zpět do zdravotnických zařízení. Tento vývoj byl vysvětlován několika faktory. Dialyzační monitor v domácnosti slouží pouze jednomu pacientovi, zatímco v dialyzačním středisku může jeden přístroj sloužit dvěma až třem pacientům denně. Navíc tehdejší přístroje byly i pro domácí prostředí poměrně velké a jejich obsluha byla často obtížná. Dialyzační program se tak v průběhu desetiletí vyvíjel jako na pomyslné houpačce – období rozvoje střídalo období útlumu („rise and fall“).
V současnosti je domácí hemodialýza v USA považována za jednu z léčebných modalit a nerozlišuje se přísně, zda je prováděna v soukromém bytě, v domě s pečovatelskou službou, nebo v domově pro seniory. Při domácí hemodialýze se systém snaží zajistit také finanční podporu pro členy rodiny nebo nabídnout pacientovi po hospitalizaci možnost přechodného pobytu ve zdravotnickém zařízení, aby rodina nebyla nadměrně zatížena péčí. Od roku 2000 se podíl domácí hemodialýzy ve světě pohybuje přibližně mezi 2–3 %. Vyšší podíl (kolem 5 % nebo více) je v zemích s řídce osídlenými oblastmi a velkými vzdálenostmi od dialyzačních center, například v Kanadě, Austrálii, na Novém Zélandu a také v některých severských zemích Evropy (Dánsko, Švédsko, Norsko). Japonsko tuto metodu rovněž používá, ale přesná čísla nejsou vždy uváděna. V USA se podíl domácí hemodialýzy pohyboval v období let 1973–2020 přibližně mezi 40 % a 10 %. Hongkong uvádí podíl kolem 3 %, v České republice přibližně 1,4 %, zatímco některé další státy domácí hemodialýzu nenabízejí.
Celkově lze říci, že podíl domácí hemodialýzy ve světě v posledních letech pozvolna roste. Přesto však v domácím režimu stále jednoznačně dominuje peritoneální dialýza, která představuje přibližně 11,6 % dialyzační léčby.
Erytropoetin
Erytropoetin zásadně změnil kvalitu života dialyzovaných pacientů. Po úpravě doprovodné anémie tímto lékem postupně vymizely mnohé „uremické projevy“, které byly dříve u pacientů běžné.
Historie erytropoetinu je však poměrně dlouhá. Začala již v 50. letech 20. století, kdy hematolog L. O. Jacobson vyzval amerického biochemika E. Goldwassera (1922–2010), aby zahájil hledání látky podporující tvorbu červených krvinek. Goldwasser začal systematicky zkoumat jednotlivé orgány laboratorních zvířat a v roce 1957 zjistil, že tato stimulující látka vzniká v ledvinách. Následujících 15 let sbíral moč od pacientů s aplastickou anemií. Celkem shromáždil přibližně 2 500 litrů moči, ze které se mu společně s japonským vědcem Takajim Miyakem podařilo izolovat pouhých 8 mg erytropoetinu. Goldwasser následně podal patentovou přihlášku na izolovaný erytropoetin a získaný materiál poskytl výzkumníkům společnosti Amgen. Výzkumný tým vedený Fu‑Kuen Linem následně identifikoval gen pro erytropoetin a pomocí metod genetického inženýrství vytvořil rekombinantní epoetin alfa (Epogen). Tento lék byl uveden na trh v roce 1989. V roce 1991 publikoval profesor J. W. Eschbach přehledný článek „Erythropoietin 1991“, který významně přispěl k rozšíření poznatků o této léčbě.4 Prof. Eschbach o erytropoetinu často přednášel na nefrologických kongresech a byl považován za vynikajícího řečníka. Dnes je erytropoetin dostupný všem pacientům, kteří jej potřebují. V 90. letech však byl tento lék přidělován jednotlivým hemodialyzačním střediskům v omezeném množství. Později se jeho použití rozšířilo také na pacienty v predialyzační nefrologické ambulantní péči, což výrazně zlepšilo jejich kvalitu života.
Během desetiletí se změnil také způsob podávání erytropoetinu (intravenózně i subkutánně) i intervaly mezi jednotlivými dávkami – od aplikace jednou týdně až po podání jednou měsíčně. Jedinou negativní zprávou v souvislosti s tímto lékem bylo jeho zneužívání ve sportu, protože erytropoetin je zařazen na seznam zakázaných dopingových látek.
Jak je to s hemodialyzační léčbou ve světě?
Statistické údaje o dialyzační léčbě se rychle mění a existují z různých pohledů, takže lze nalézt řadu přehledů s odlišnými daty o léčbě hemodialýzou a dalších metodách náhrady funkce ledvin.5 Zajímavé jsou například údaje z roku 2020 prezentované na konferenci Global Dialysis Market v Dublinu. Podle těchto dat bylo na světě přibližně 4 miliony pacientů léčených náhradou funkce ledvin, zejména hemodialýzou a transplantací ledviny. Hemodialýza je přitom nejčastější léčebnou metodou a představuje přibližně 90 % globálního dialyzačního trhu. Evropské země tvoří druhou největší oblast dialyzační léčby, avšak nejrychlejší nárůst počtu pacientů je zaznamenáván v Číně a Indii. Prevalence dialyzovaných pacientů se mezi jednotlivými státy výrazně liší – v USA a Japonsku přesahuje 1 000 pacientů / 1 milion obyvatel, zatímco v mnoha rozvojových zemích je léčeno méně než 100 pacientů / 1 milion obyvatel.
Odhady pro rok 2030 předpokládají, že počet pacientů léčených hemodialýzou dosáhne přibližně 5,4 milionu. Celkově populace stárne, zvyšuje se věk dialyzovaných pacientů a současně narůstá i incidence diabetu. Lze proto předpokládat, že v budoucnu bude přibývat nových pacientů indikovaných k hemodialyzační léčbě, kteří však budou věkově starší a častěji diabetici, což může negativně ovlivňovat výsledky dialyzační terapie. Podle údajů National Kidney Foundation je na světě léčeno přes dva miliony pacientů hemodialýzou nebo transplantací ledviny. Největší počet pacientů je soustředěn v pěti zemích – USA, Japonsku, Německu, Brazílii a Itálii – které však představují pouze přibližně 12 % světové populace. Naproti tomu ve více než 100 zemích, kde žije asi 50 % světové populace, je léčeno pouze kolem 20 % pacientů s terminálním selháním ledvin. Osmdesát procent všech léčených pacientů pochází z ekonomicky vyspělých zemí s dobrým přístupem ke zdravotní péči a současně s vysokým podílem starší populace.
Čeho se dočkáme v budoucnosti aneb nečekáme už moc dlouho?
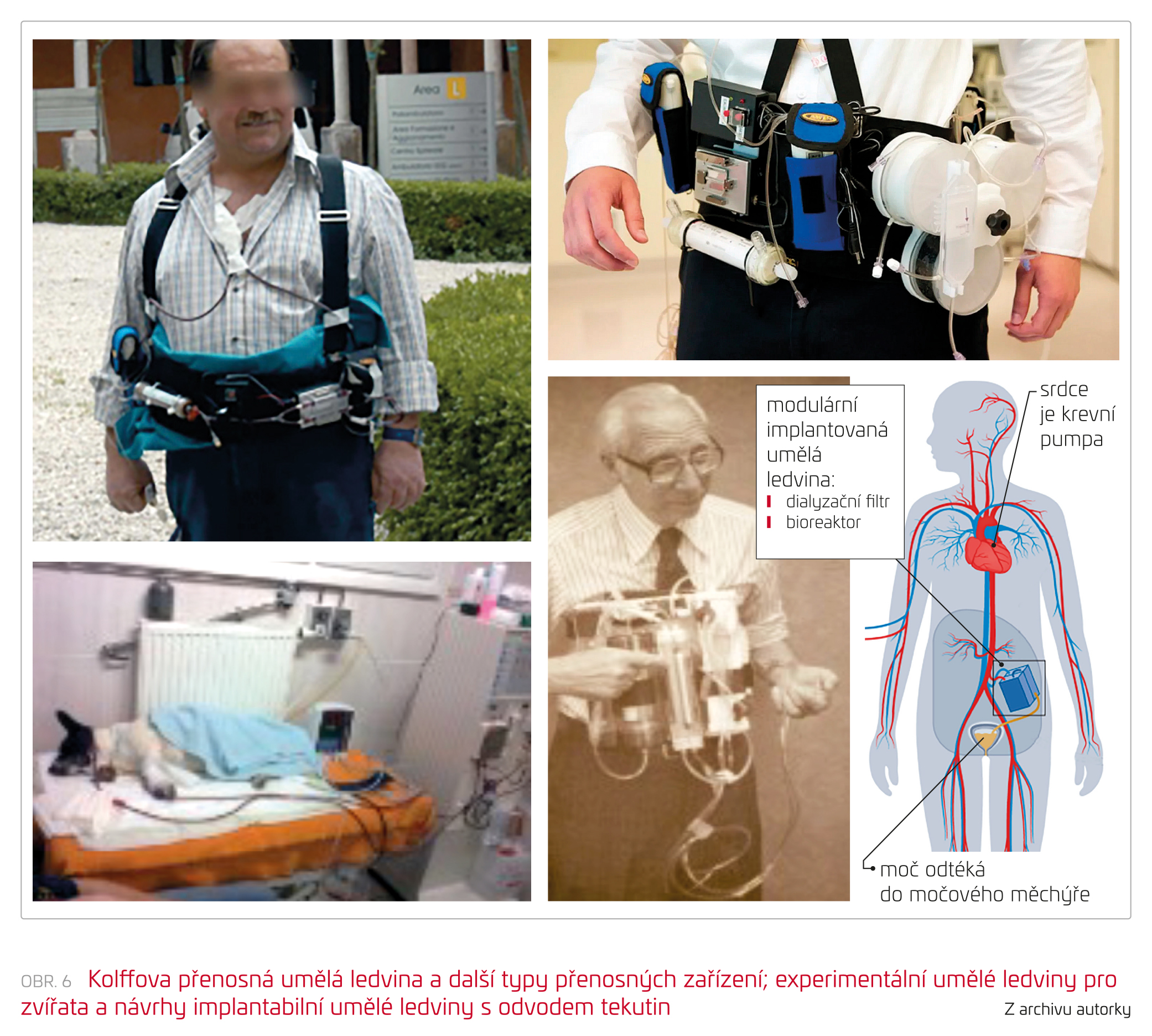
Miniaturní dialyzační monitor – přenosné zařízení – představil již v roce 1975 profesor Kolff, když ukázal svou přenosnou umělou ledvinu (obr. 6). Od té doby se o podobných projektech objevují zprávy již několik desetiletí, zatím však zůstávají převážně ve fázi experimentu. Velmi zajímavou myšlenkou je také implantabilní umělá ledvina. Její realizace je však zatím pravděpodobně v nedohlednu.
Závěr aneb kam dospěla umělá ledvina po 80 letech vývoje?
Na tuto otázku výstižně odpovídá i za mě americká profesorka J. E. Flythe.6 Současná podoba léčby nedosahuje cílů zakladatelů, tj. zajištění plné rehabilitace a příjemného života. Současná hemodialýza zhoršuje kvalitu života i zkracuje jeho délku. V průběhu let se hemodialýza odklonila od individualizovaných preskripcí z raných let a došlo ke standardizaci metody. Zatímco dříve byla hemodialýza zaměřena především na člověka, dnes je často zaměřena spíše na čísla. Máme před sebou ještě dlouhou cestu, než budeme schopni pacientům zajistit kvalitu života, jakou si zaslouží. Realizace inovací záleží na odhodlání nových generací, které musejí porozumět minulosti, aby mohly formulovat budoucnost. Jak to formuloval americký autor sci‑fi Robert A. Heinlein, „Generace, která ignoruje historii, nemá ani budoucnost“.
Literatura
- Henderson LW, Besarab A, Michaels A, Bluemle LW Jr. Blood purification by ultrafiltration and fluid replacement (diafiltration). Hemodial Int 2004;8:10–18.
- Yoshida M, Maeoka Y, Takahashi A, et al. Effect of HDF versus HD on vascular access patency when starting HD. Nephrol Dial Transplant 2025;40:1538–1549.
- Blagg CR. The early history of dialysis for chronic renal failure in the United States: a view from Seattle. Am J Kidney Dis 2007;49:482–496.
- Eschbach JW. Erythropoietin 1991 – overview. Am J Kidney Dis 1991;18:3–9.
- United States Renal Data System (USRDS). USRDS 2023 Annual Data Report: Epidemiology of Kidney Disease in the United States. Bethesda, MD: National Institutes of Health, National Institute of Diabetes and Digestive and Kidney Diseases; 2023 [online]. Dostupné z: https://usrds‑adr.niddk.nih.gov/2023
- Flythe JE. Dialysis – Past, present, and future: A Kidney360 Perspectives Series. Kidney360 2023;4:567–568.
- Kategorie: Názor hosta
- Klíčová slova: dialyzační roztok; dialyzační technologie; domácí hemodialýza ; hemodiafiltrace; hemodialýza; transplantace ledvin